Kapitel 14: Ionen, Salze, Fällungsreaktionen und Ionenbindung

Ein Natriumchloridkristall
Vorbemerkungen
In diesem Kapitel erweitert sich Dein chemisches Wissen enorm! Du lernst eine neue Gruppe von Verbindungen kennen, die Salze. Salze und auch salzähnliche Stoffe wie die Oxide haben einen besonderen Aufbau. Sie bestehen aus Ionen. Man spricht auch von ionogenen Verbindungen.
Ionen sind keine Elemente und müssen von Dir immer gut von diesen unterschieden werden. Achte also von nun an darauf, mit welchen Stoff Du es jeweils zu tun hast: Element, Ion oder Verbindung.
Es ist ein schweres Kapitel!
Ich habe das Kapitel in folgende Unterkapitel aufgeteilt:
I: Ionen und die Ionenbindung
II: Salze und Mineralien
III: Der Aufbau von Salzkristallen und energetische Aspekte der Salz- und Ionenbildung
IV: Fällungsreaktionen und chemische Nachweise
V: Zusammenfassung, Tipps und wichtige Hilfen
Unterkapitel I: Ionen und die Ionenbindung
Leitfähigkeitsmessung von Lösungen
Ganz am Anfang dieses Kurses haben wir die Leitfähigkeit von Elementen gemessen. Metalle hatten wir damals festgestellt leiten den elektrischen Strom in der Regel gut. Was ist aber mit Lösungen?
V1: In Wasser werden verschiedene Salze (NaCl, KCl, Na2SO4) sowie Harnstoff und Zucker gegeben. Es sollte immer die gleiche Flüssigkeitsmenge zugegeben werden und auch die gleiche Menge Feststoff. Die Leitfähigkeit wird dann gemessen.

Beobachtungen:
|
wässrige Lösung von |
|||||||||
|
Dest. Wasser |
Leitungswasser |
NaCl |
NaNO3 |
KCl |
Na2SO4 |
CaCO3 |
Harnstoff |
Zucker |
|
|
Leitfähigkeit |
sehr gering |
gering |
++ |
++ |
++ |
++ |
gering |
- |
sehr gering |
|
Mögliche Werte bei 3V |
0,03 |
15 |
1500 |
1650 |
1400 |
800 |
90 |
0,03 |
0,03 |
Zusatzversuch: Leitfähigkeit eines Salzkristalls:
V2: Messung der Leitfähigkeit von festen Salzen (=Kristallen)
B2: Die festen Salze leiten den elektrischen Strom gar nicht!
Schlussfolgerungen:
Wenn man nicht immer die gleiche Salzmenge zugibt oder das Wasservolumen unterschiedlich ist, hat man keine absolut vergleichbaren Ergebnisse. Die Ergebnisse können also ungenau sein. Trotzdem kann man verschiedene Zusammenhänge gut erkennen:
1. Je mehr Salz in das Wasser zugegeben wird, desto höher ist die Leitfähigkeit.
2. Festes Salz und Salze, die sich nicht auflösen, zeigen keine Leitfähigkeit.
3. Wasser zeigt nur eine sehr geringe Leitfähigkeit.
Weißt Du eigentlich (noch), was Leitfähigkeit eigentlich ist?
Unsere Apparatur misst eigentlich die Stromstärke [I]. Sie gibt an, wie viele Elektronen durch die Lösung vom Minuspol zum Pluspol wandern. Die Leitfähigkeit ist definiert als die Proportionalitätskonstante zwischen der Stromdichte und der elektrischen Feldstärke.
Wie gelangen nun die Elektronen vom Minuspol zum Pluspol?
Salze zerfallen beim Lösen in geladene Teilchen. Diese geladenen Teilchen transportieren die Ladungen des elektrischen Stroms von der ersten Elektrode durch das Wasser zur zweiten Elektrode.
Dabei kann man sich vorstellen, dass sie die Elektronen „tragen“, wie ein Wanderer einen Rucksack trägt. Da das altgriechische Wort für Wanderer „ionos“ lautet, nennen die Chemiker alle geladenen Teilchen Ionen. Im Kochsalz (NaCl) sind geladene Natriumionen und Chloridionen vorhanden.
Je mehr Salz sich dabei auflöst, desto mehr erhöht sich die Leitfähigkeit, da mehr Ionen in der Lösung vorhanden sind.
Leitungswasser leitet übrigens auch minimal den elektrischen Strom, da in ihm winzige Mengen von Mineralsalzen enthalten sind. Zucker und Harnstoff hingegen sind keine Salze! Sie bestehen nicht aus Ionen und leiten deshalb den elektrischen Strom nicht.
Warum leitet nun der Feststoff den elektrischen Strom nicht? Sind im Kristall keine Ionen vorhanden?
Salze sind aus Ionen aufgebaut. In der Lösung (sowie in geschmolzener Form) sind die Ionen frei beweglich und können Ladungen transportieren, im Feststoff sind die Ionen bereits vorhanden, aber sie sind nicht beweglich!
Elektrischer Strom ist der Fluss von e–.
Nur in Salzlösungen und Salzschmelzen sind die Ionen beweglich.
=> Salzkristalle leiten den elektrischen Strom nicht.
Ionen sind elektrisch geladene Atome oder Moleküle.
Ionen mit positiver Ladung werden Kationen genannt, Ionen mit negativer Ladung Anionen.
Ionenwanderung
V: Das mit Natriumchloridlösung getränkte Filterpapier, wird an den Enden mit einem gefaltetem Kupferblech und einer Krokodilklemme an die Gleichspannungsquelle angeschlossen. Auf der Filterpapiermitte werden die Probesubstanzen aufgelegt (Kupfersulfat, Kaliumdichromat und Kaliumpermanganatkristalle). Bestimme die mittlere Ionenwanderungsgeschwindigkeit.
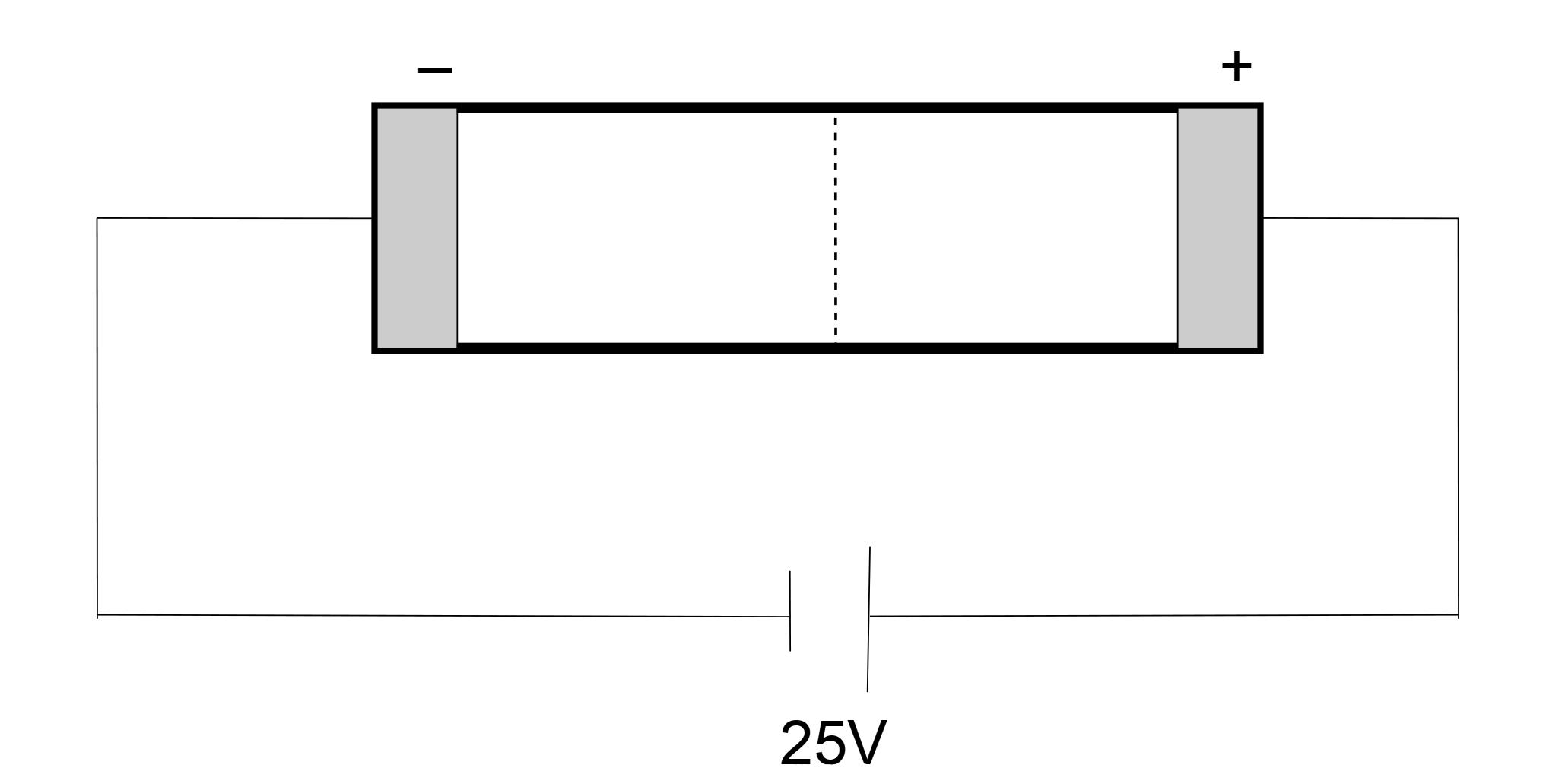
Kathode
<---- Kupferionen wandern nach links
Kationen sind positiv geladen
Anode
Chromat- und Manganationen wandern nach rechts --->
Anionen sind negativ geladen
B: Zum Pluspol sieht man eine orange und violette Färbung, zum Minuspol eine blaue.
S: Unter dem Einfluss des elektrischen Feldes wandern die positiv geladenen (Kationen) Kupferionen zum Minuspol (Kathode), die negativ geladenen Chromationen (Anionen) wandern zum Pluspol (Anode).
Einige der verwendeten Ionen haben eine typische Farbe: Manganationen sind pink, Kuper(II)ionen sind hellblau und Dichromationen sind gelb: KMnO4, CuSO4, K2Cr2O7
Auf der Seite des Minuspols sieht man nun die blauen Kupferionen, auf der anderen Seite die beiden Säurerestionen. Kannst Du nun eine Vorhersage zu den Ladungen der Ionen treffen?
Edelgaskonfiguration
Man liest oft die folgende Vereinfachung:
Edelgase sind die Elemente der 8. Hauptgruppe. Sie sind sehr reaktionsträge, was durch ihre vollbesetzte äußere Elektronenhülle verursacht ist.
Das ist für Wasserstoff und Helium mit zwei Elektronen richtig. Auch für Elemente der 2. Periode ist die äußere Hülle voll besetzt und somit Edelgaskonfiguration erreicht (Oktett).
Das Problem dieser Vereinfachung ist, dass ab der dritten Periode mehr Elektronen in die äußeren Hüllen passen!
Eine Elektronenhülle kann genau 2n2 Elektronen aufnehmen. (n= Periodennummer = Anzahl an Elektronenhüllen)
=> Elemente der 1. Periode haben mit 2 e– Edelgaskonfiguration.
=> Elemente der 2. Periode haben mit 8 e– Edelgaskonfiguration.
=> Elemente der 3. Periode haben mit 8 e– Edelgaskonfiguration, können aber 18 e– aufnehmen.
=> Elemente der 4. Periode haben mit 8 e– Edelgaskonfiguration, können aber 32 e– aufnehmen.
=> Elemente der 5. Periode haben mit 8 e– Edelgaskonfiguration, können aber 50 e– aufnehmen. Usw.
Wie kann man nun die Edelgaskonfiguration genau beschreiben?
Edelgaskonfiguration ist die Konfiguration mit 2 Valenzelektronen für Wasserstoff und Helium sowie 8 Valenzelektronen für alle Hauptgruppenelemente (s2p6)! Davon leitet sich auch der Begriff „Oktettregel“ ab.
Für Nebengruppenelemente und Komplexe gilt stattdessen, dass sie 18 Valenzelektronen einen besonders stabilen Zustand erreichen.
Edelgase sind besonders reaktionsträge und chemisch sehr stabil.
Es existieren nur wenige bekannte Verbindungen (z.B. XeF6).
Die Edelgase haben im elementaren Zustand bereits ihre Edelgaskonfiguration. Durch diese besondere Konfiguration haben einen besonders energiearmen Zustand, dadurch sind sie chemisch besonders stabil und reaktionsträge.
Edelgase sie sind im elementaren Zustand einatomig und bilden nur in Ausnahmefällen Edelgasverbindungen.
Zusatzinformationen:
- https://de.wikipedia.org/wiki/Helium
- https://de.wikipedia.org/wiki/Neon
- https://de.wikipedia.org/wiki/Argon
- https://de.wikipedia.org/wiki/Krypton
- https://de.wikipedia.org/wiki/Xenon
- https://de.wikipedia.org/wiki/Radon
- https://de.wikipedia.org/wiki/Edelgaskonfiguration
- https://de.wikipedia.org/wiki/18-Elektronen-Regel
- https://de.wikipedia.org/wiki/Oktettregel
Welche Ionen sind in Natriumchlorid zu finden?
a) Bildung des Na- Ions
Zeichne das Natriumatom 2311Na (es hat 1 Außenelektron):
Die wichtigste Frage, die man sich bei der Bestimmung der Ionenladung immer stellen muss:
Was muss passieren, damit eine vollbesetzte Außenelektronenwolke vorliegt (also Edelgaskonfiguration erreicht wird!)?
Das Element Natrium muss zum Erreichen der Edelgaskonfiguration dieses eine Außenelektron abgegeben! Dem verbleibende Teilchen fehlt es nun, aber die darunterliegende Elektronenhülle, die ja nun die äußerste ist, ist vollbesetzt. Das neu entstandene Ion ist nun positiv geladen.
2311Na - Atom 2311Na+- Ion
11p+, 11e–, 12n 11p+, 10e–, 12n
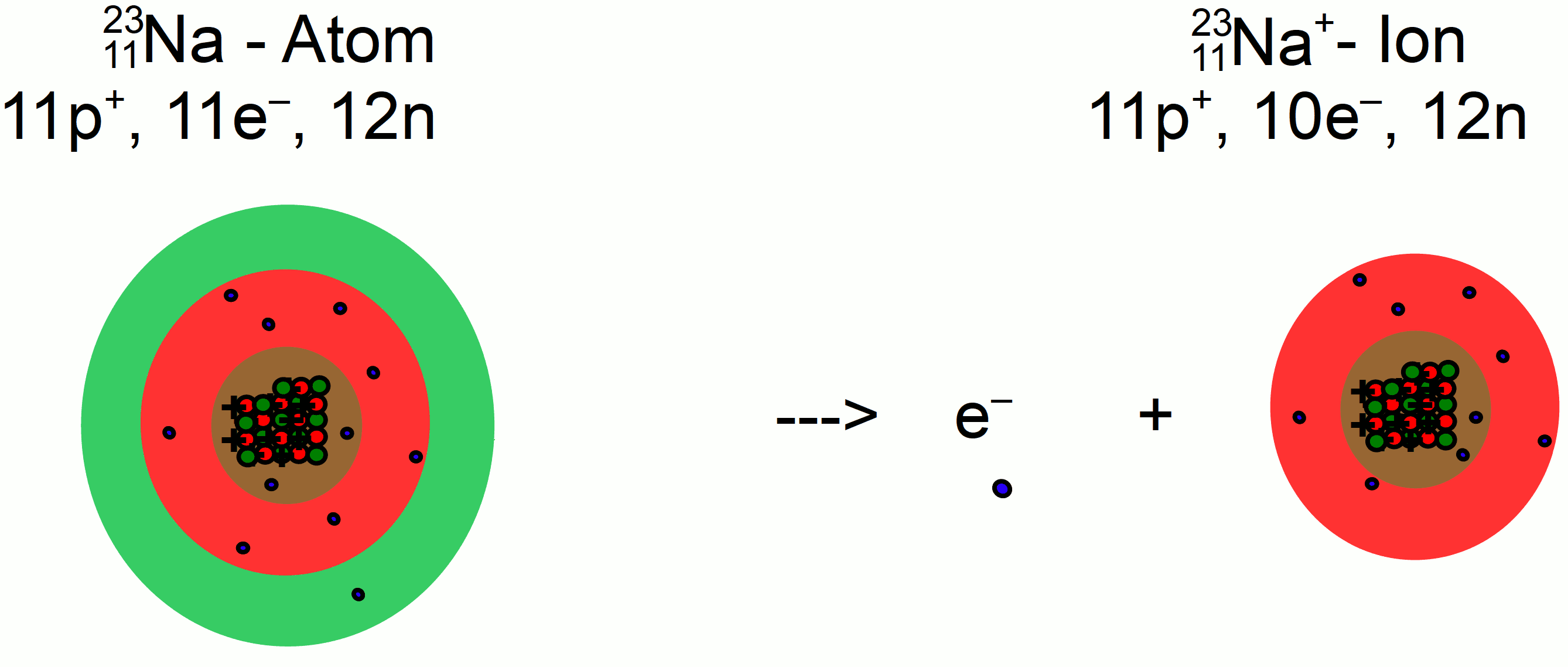
Wie genau kommt es zur positiven Ladung?
In der atomaren Form liegen je 12 negative und 12 positive Ladungen vor. Entfernt man ein negatives Elektron, dann bleibt eine positive Ladung „über“.
=> Das Ion ist also einfach positiv geladen.
Hinweis: In Reaktionsgleichungen werden keine Elektronen „abgezogen“ oder „subtrahiert“. Für die Gleichung wird stattdessen von einer „Aufspaltung“ in Elektron und Ion ausgegangen.
b) Bildung des Chlorid-Ions
Zeichne das Chloratom 3517Cl (es hat 7 Außenelektronen):
Was muss passieren, damit eine vollbesetzte Außenelektronenwolke vorliegt?
Ein Außenelektron wird aufgenommen. Das neue Teilchen hat nun ein Elektron mehr und somit eine negative Ladung mehr als vorher. Dadurch ist es negativ geladen.
3517Cl - Atom 3517Cl– - Ion
17p+, 17 e–, 18n 17p+, 18 e–, 18n
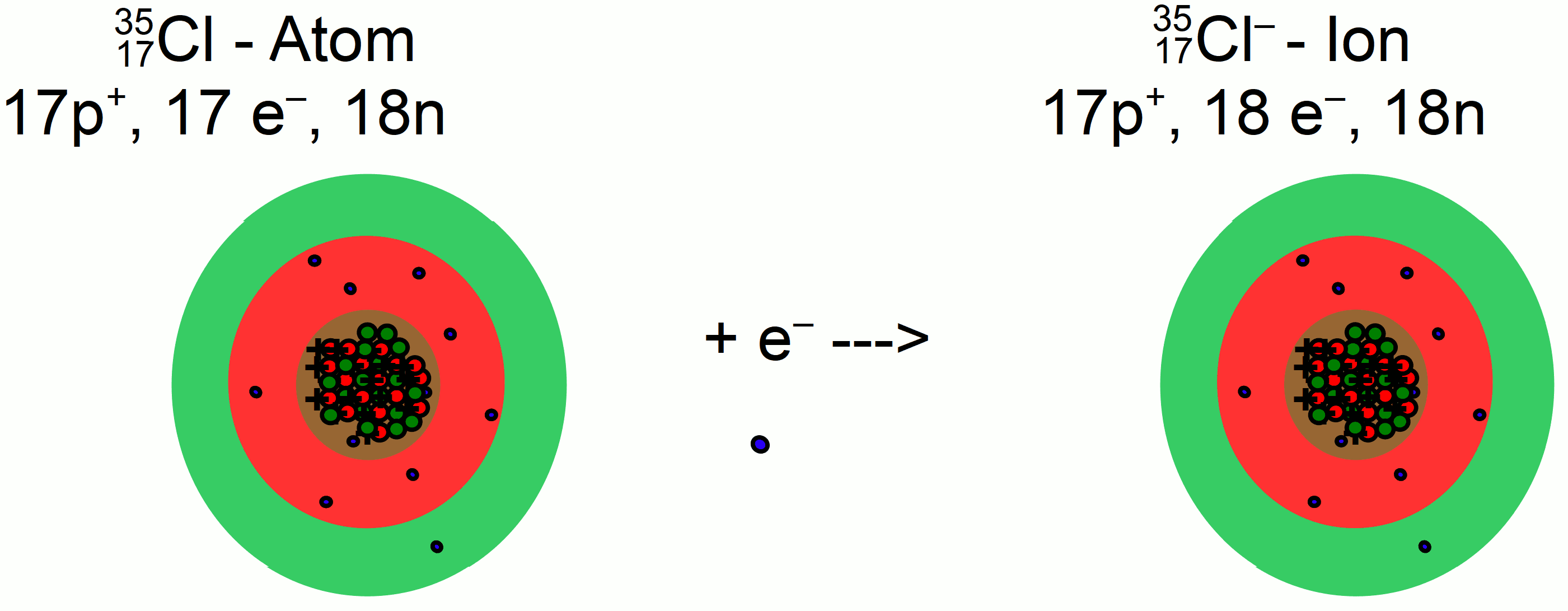
Wie kommt es zur negativen Ladung?
In der atomaren Form liegen je 17 negative und 17 positive Ladungen vor. Fügt man nun ein negatives Elektron hinzu, dann liegt eine negative Ladung im Überschuss vor.
=> Das Ion ist also einfach negativ geladen.
Fast jedes Element kann sowohl atomar, als auch in ionogener Form auftreten.
Salze sind aus Ionen aufgebaut.
Aufgaben: Bestimme die Ionenladung der folgenden Ionen: a) LiF, b) MgO, c) HCl, d) CaF2
Erklärung nach den Besetzungsregeln des Orbitalmodells (falls im UR schon gemacht)
Es gibt für die Oberstufe noch ein anderes, schwierigeres aber besseres Atommodell, das Orbitalmodell. Oft zeichnet man hier die Elektronenhüllen nicht, sondern ordnet die Elektronen in sogenannten „Besetzungsdiagrammen“ an, welche die unterschiedlichen Energieniveaus zeigen.
Bildung des Natriumions:
Elemente „streben“ vollbesetzte Energieniveaus an. Natrium erreicht dies durch Abgabe eines Elektrons und erreicht so die Edelgaskonfiguration s2p6:

Welche Ladung wird das Natriumion also tragen, damit es nur vollbesetzte Energieniveaus hat?
=> +1 => Na+
Vergleiche:
|
Natriumatom |
Natriumion, Na+ |
|
11 Elektronen, davon 1 Valenzelektron |
10 Elektronen, davon 8 Valenzelektron |
|
=> keine voll besetzte Valenzelektronenhülle |
=> voll besetzte Valenzelektronenhülle |
|
=> chemisch eher instabil und reaktiv |
=> stabilerer Zustand (energetisch günstiger) |
|
=> wenig reaktiv |
Bildung des Chlorions
Chlor erreicht Edelgaskonfiguration durch Aufnahme eines Elektrons und erreicht so die Edelgaskonfiguration s2p6:

Welche Ladung kann ein Chloridion tragen, damit es nur vollbesetzte Energieniveaus hat?
=> -1 => Cl–
Vergleiche:
|
Chloratom |
Chloridion |
|
17 Elektronen, davon 7 Valenzelektron |
16 Elektronen, davon 8 Valenzelektron |
|
=> keine voll besetzte Valenzelektronenhülle |
=> voll besetzte Valenzelektronenhülle |
|
=> chemisch sehr reaktiv |
=> stabilerer Zustand (energetisch günstiger) |
|
=> wenig reaktiv |
Man kann nun nicht jedes Mal komplette Atome bzw. Besetzungsdiagramme zeichnen, um die Ladung eines Ions zu bestimmen. Zum Glück hilft uns das Periodensystem der Elemente da weiter:
Zur Bestimmung der Ionenladung helfen ein paar Regeln und Tipps mithilfe des PSE:
Oberstes Gebot: Die Anzahl an Valenzelektronen des ungeladenen Atoms bestimmt die Ionenladung. Diese Anzahl ist entscheidend, ob Elektronen aufgenommen oder abgegeben werden. Ziel ist dabei i.d.R. Edelgaskonfiguration.
-
Die Ladung einatomiger Ionen entspricht bei Elementen der 1.- 3. Hauptgruppe der Hauptgruppennummer.
Die Elemente der 1. Hg bilden 1fach positive Ionen (z.B.: Li ---> Li+ + e–)
Die Elemente der 2. Hg bilden 2fach positive Ionen (z.B.: Ca ---> Ca2+ + 2e–)
Die Elemente der 3. Hg bilden oft 3fach positive Ionen (z.B.: Al ---> Al3+ + 3e–)
Der Name dieser Ionen entspricht dem Elementnamen mit hinzugefügtem Wort „-Ion“. z.B. Lithium-Ion, Calcium-Ion. Diese Ionen sind alle positiv geladen, sie heißen Kationen.
Bei den restlichen Elementen kann sie der Anzahl an Elektronen entsprechen, die zum Erreichen von vollständig besetzten Energiestufen aufgenommen (oder abgegeben werden) müssen:
Bsp. Sauerstoff hat 6 VE => zur vollbesetzten Energiestufe fehlen 2 e– => O2– - Ion
Elemente der 7. Hg bilden oft 1fach negative Ionen (wenn sie überhaupt Ionen bilden) (z.B.: Cl ---> Cl– + e–)
Elemente der 6. Hg bilden oft 2fach negative Ionen (wenn sie überhaupt Ionen bilden) (z.B.: O ---> O2– +2e–)
Elemente der 5. Hg bilden oft 3fach negative Ionen (wenn sie überhaupt Ionen bilden) (z.B.: N ---> N3– + 3e–)
Der Name der Ionen dieser Hauptgruppen endet auf die Silbe „-id“, aber nur, wenn sie auch der genannten Regeln folgen! z.B. Chlorid, Sulfid, Oxid, Calcium-Ion.
Aber Achtung! Es gibt weitere Ionen der 5.-7. Hauptgruppe. Sie tragen dann andere Namen.z.B. Chlorat, Oxonium usw. Diese Namen musst Du noch nicht kennen.
Alle negativen Ionen werden auch Anionen genannt. -
Metalle bilden positive geladene Ionen (= Kationen), Nichtmetalle bilden (wenn sie Ionen bilden) negativ geladene Ionen (=Anionen).
-
Nebengruppenelemente (Fe, Cu, Zn) bilden „Kationen“ verschiedener Ladungen. Häufig ist ihre Ladung 2+.
-
Edelgase bilden keine Ionen.
Aufgaben:
-
Vervollständige: Ionen entstehen durch...
-
Na+-Ionen unterschieden sich von Na-Atomen durch...
-
Welche Eigenschaften haben Ionen?
-
Erkläre den Begriff Ionenbindung.
-
Wie bestimmt man die Ladung eines Säurerestes?
-
Welche Voraussetzungen müssen gegeben sein, damit Ionen den Strom leiten?
-
Schlage im Periodensystem nach, wie sich die Atom- und Ionenradien bei drei von Dir gewählten Elementen unterscheiden.
-
Bestimme die Ionenladungen der folgenden Teilchen:
Na; Cl, Mg; Li; Sr; Be; S; O; Al; O; C; H; K; Ca; Ba; Br; I; F; Ne -
Wie lautet die richtige Formel für folgende Salze; Natriumchlorid (= Kochsalz); Bariumsulfat; Magnesiumcarbonat; Natriumsulfat; Lithiumnitrat; Kaliumbromid; Calciumphosphat; Aluminiumsulfat.
Welche Ionenladung hat das Wasserstoffion?
Wasserstoff hat ein nur ein einziges Elektron. Es kann es zum Erreichen der vollbesetzten Außenelektronenwolke und somit zum Erreichen der Edelgaskonfiguration ein Elektron aufnehmen oder eines abgeben.
11H

Hydridion H– H-Atom Proton H+
Während einige Metalle mit dem Hydrid Verbindungen eingehen, so ist (v.a. in der Schule) das H+ der häufigere Reaktionspartner.
Ionen verbinden sich miteinander: Die Ionenbindung
Vom Magnetismus aus dem Physikunterricht kennst Du die Anziehung der unterschiedlichen Pole und die Abstoßung von gleichsinnigen Polen. In der Chemie hast Du nun positive und negative elektrostatische Ladungen bei Ionen kennengelernt. Auch diese ziehen sich bei unterschiedlichem Vorzeichen an und stoßen sich bei gleichem Vorzeichen ab.
Verbindungen unterschieden sich von Elementen dadurch, dass in Ihnen mehrere Elemente miteinander verbunden sind. Grundsätzlich gibt es zwei verschiedene Arten, wie sich Elemente miteinander verbinden können. Die Atombindung lernst Du in einem der folgenden Kapitel. Die andere Art ist die Ionenbindung.
Die Verbindung mehrerer Elemente kommt durch ihre unterschiedliche Ladung zustande:
Natriumchlorid: Na+Cl–
Calciumfluorid: Ca2+F–2
Aluminiumbromid: Al3+Br–3
(Die Ladungen werden bei Salzen in der Regel nicht notiert, aber gerade am Anfang, kann man dies machen, da es eine Hilfe sein kann. Aber es müssen dann immer beide Ladungen notiert werden!)
Eine solche Verbindung durch gegensätzliche Ionenladungen wird Ionenbindung oder ionogene Verbindung genannt.
Ionen ungleicher Ladung ziehen sich an und verbinden sich.
H+ + Cl– ---> H+Cl–
Na+ + Cl– ---> Na+Cl–
Mg2+ + O2– ---> Mg2+O2–
Dabei müssen positive und negative Ladungen ausgeglichen sein, sodass die entstehende Verbindung „nach außen“ ungeladen ist.
2H+ + O2– ---> H+2O2–
2Al3+ + 3O2– ---> Al3+2O2–3
Die Verbindung von Ionen zu einer Verbindung nennt man Ionenbindung.
Die Ionenbindung kommt bei allen Salzen vor. Dies ist eine sehr große Gruppe innerhalb der anorganischen Chemie. Bei Salzen ist diese Art der Bindung sehr fest. Sie kann durch Wasser oft aber „gelöst“ werden. Bei Salzen entsteht so eine Salzlösung.
Alle Salze bestehen aus Ionen, welche durch eine Ionenbindung miteinander verbunden sind.
Es gibt noch eine zweite Art der Verbindung zwischen Atomen. Sie wird Atombindung genannt. Du lernst sie später kennen.
Beispiele für Metallionen und Säurerestionen:
|
Metallion |
Säurerestion |
Name des Säurerests |
|
Lithium: Li+ |
Cl– |
Chlorid |
|
Kalium: K+ |
F– |
Fluorid |
|
Natrium: Na+ |
Br– |
Bromid |
|
Magnesium: Mg2+ |
I– |
Iodid |
|
Calcium: Ca2+ |
S2– |
Sulfid |
|
Barium: Ba2+ |
(NO3)– |
Nitrat |
|
Aluminium: Al3+ |
(SO4)2– |
Sulfat |
|
Kupfer: Cu2+ |
(SO3)2– |
Sulfit |
|
Silber: Ag+ |
(CO3)2– |
Carbonat |
|
Eisen: Fe3+ |
(PO4)3– |
Phosphat |
Aufgaben:
Trage alle Ionenladungen der Säurereste in der Tabelle (oder dem auf dem Säurezettel des letzten Jahres) ein!
Hier die korrekte Lösung:
|
Die wichtigsten Säuren und ihre Säurereste |
|
Säure: |
Säurerest: |
||
|
HF |
Fluorwasserstoffsäure |
F– |
Fluorid |
|
HCl |
Chlorwasserstoffsäure |
Cl– |
Chlorid |
|
HBr |
Bromwasserstoffsäure |
Br– |
Bromid |
|
HI |
Iodwasserstoffsäure |
I– |
Iodid |
|
H2S |
Schwefelwasserstoff(säure) |
S2– |
Sulfid |
|
HCN |
Blausäure |
CN– |
Cyanid |
|
HNO3 |
Salpetersäure |
(NO3)– |
Nitrat |
|
H2SO4 |
Schwefelsäure |
(SO4)2– |
Sulfat |
|
H2CO3 |
Kohlensäure |
(CO3)2– |
Carbonat |
|
H3PO4 |
Phosphorsäure |
(PO4)3– |
Phosphat |
|
HNO2 |
Salpetrigesäure |
(NO2)– |
Nitrit |
|
H2SO3 |
Schwefeligesäure |
(SO3)2– |
Sulfit |
|
H3PO3 |
Phosphorigesäure |
(PO3)3– |
Phosphit |
Liste wichtiger Anionen
|
(SO4)2-– |
Sulfat |
(NO3)– |
Nitrat |
(ClO4)– |
Perchlorat |
||
|
(HSO4)– |
Hydrogensulfat |
(NO2)– |
Nitrit |
(ClO3)– |
Chlorat |
||
|
(SO3)2– |
Sulfit |
||||||
|
(S)2– |
Sulfid |
(NH4)+ |
Ammonium |
(MnO4)– |
Permanganat |
||
|
(S2O3)2– |
Thiosulfat |
||||||
|
(PO4)3– |
Phosphat |
(CrO4)2– |
Chromat |
||||
|
(CO3)2– |
Carbonat |
(HPO4)2– |
Hydrogenphosphat |
(Cr2O7)2– |
Dichromat |
||
|
(HCO3)– |
Hydrogencarbonat |
(H2PO4)– |
Dihydrogenphosphat |
Für Schüler der Oberstufe: Bezeichnung wichtiger Anionen
a) Einatomige Anionen
|
Ion |
Name |
Säurename |
|
H+ |
Hydrid |
|
|
F–, Cl–, Br–, I– |
Fluorid, Chlorid, Bromid, Iodid (allg. Halogenid) |
Fluorwasserstoffsäure, Chlorwasserstoffsäure, Bromwasserstoffsäure, Iodwasserstoffsäure |
|
O2– |
Oxid |
Wasser (!) |
|
S2– |
Sulfid |
Schwefelwasserstoffsäure |
b) Mehratomige Anionen
|
(AsO4)3– |
Arsenat |
Arsensäure |
|
(AsO3)3– |
Arsenit |
Arsenige Säure |
|
(BO3)3– |
Borat |
(Ortho-)Borsäure |
|
(CH3COO)– |
Acetat |
Essigsäure |
|
(CN)– |
Cyanid |
Hydrogencyanid (Blausäure) |
|
(CO3)2– |
Carbonat |
Kohlensäure |
|
(ClO4)– |
Perchlorat |
Perchlorsäure |
|
(ClO3)– |
Chlorat |
Chlorsäure |
|
(ClO2)– |
Chlorit |
Chlorige Säure |
|
(ClO)– |
Hypochlorit |
Hypochlorige Säure |
|
(Cr2O7)2– |
Dichromat |
„Dichromsäure“ |
|
(CrO4)2– |
Chromat |
„Chromsäure“ |
|
(MnO4)– |
Permanganat |
„Permangansäure“ |
|
(N3)– |
Azid |
Hydrogenazid, Stickstoffwasserstoffsäure |
|
(NCO)– |
Isocyanat |
Isocyansäure |
|
(NO3)– |
Nitrat |
Salpetersäure |
|
(NO2)– |
Nitrit |
Salpetrige Säure |
|
(OCN)– |
Cyanat |
Cyansäure |
|
(OH)– |
Hydroxid |
Wasser! |
|
(PO4)3– |
Phosphat |
Phosphorsäure |
|
(PO3)3– |
Phosphit |
Phosphorige Säure |
|
(PO2)3– |
Phosphinat |
Phosphinsäure |
|
(SO4)2– |
Sulfat |
Schwefelsäure |
|
(SO3)2– |
Sulfit |
Schweflige Säure |
|
(S2O3)2– |
Thiosulfat |
Thioschwefelsäure |
|
(SCN)– |
Thiocyanat |
Thiocyansäure |
Übungen zur Bestimmung der Ionenladungen
a) Bestimme die Ionenladungen der folgenden Ionen:
Na; Cl, Mg; Li; Sr; Be; S; O; Al, O; C; H; K; Ca; Ba; Br; I; F; Ne
b) Wie lautet die richtige Formel für folgende Salze:
Natriumchlorid (= Kochsalz):
Bariumsulfat:
Magnesiumcarbonat:
Natriumsulfat:
Lithiumnitrat:
Kaliumbromid:
Calciumphosphat:
Aluminiumsulfat:
Unterkapitel II: Salze und Mineralien
Eigenschaften der Salze
Umgangssprachlich ist „Salz“ für viele Menschen nur ein einziger Stoff. Gemeint ist damit oft das Kochsalz (auch Steinsalz genannt) Natriumchlorid. Tatsächlich sind die Salze eine der größten Stoffgruppen der Chemie! Zu dieser Gruppe gehören Tausende von Verbindungen. Mithilfe dieses Textes wirst Du diese Gruppe besser kennenlernen.
Charakteristische Eigenschaften von Salzen:
- Salze sind aus Ionen aufgebaut. Dabei sind im festen Zustand immer positive Ionen (Kationen) mit negativen Ionen (Anionen) verbunden. Dabei ist das Verhältnis zwischen Anionen und Kationen so ausgeglichen, dass sich die Ladungen aufheben und Salze so nach „außen“ hin ungeladen sind.
- Salze sind bei Raumtemperatur Feststoffe. Sie haben einen hohen Schmelzpunkt.
- Salzkristalle sind hart und spröde. Sie brechen leicht und sind nicht biegsam.
- Salze bestehen immer aus einem oder mehreren Metallion(en) und einem oder mehreren Säurerestion(en).
- Salze haben hohe Siede- und Schmelzpunkte.
- Salze sind chemische Verbindungen, Die Vereinigung kommt durch die verschiedenen Ladungen (positive und negative Ionen) zustande.
- Das positive Ion ist (fast) immer ein Metallion (die Ausnahme ist Ammonium), das negative Ion ist immer ein Säurerest oder ein Oxid.
- Salze als Feststoffe (= Salzkristalle) leiten den elektrischen Strom nicht, da die Ionen im Kristall unbeweglich sind! Salzschmelzen und wässrige Lösungen hingegen, leiten den elektrischen Strom, da sie frei bewegliche Ionen enthalten.
- Salze haben fast ausnahmslos immer hohe Siede- und Schmelzpunkte.
- Salze können ganz verschiedene Farben haben. Kupfersalze sind z.B. oft blau. Dabei ist meist das Metallion für die Farbe verantwortlich.
- Nicht jedes Salz löst sich in Wasser auf. So sind zum Beispiel Kalk (Calciumcarbonat) und Gips (Calciumsulfat) wasserunlösliche Salze.
Entstehung von Salzen und Salzgewinnung des Menschen:
Salze sind für den Menschen unentbehrlich. Das wichtigste ist dabei das Kochsalz (Natriumchlorid). Es wurde im Mittelalter auch das „weiße Gold genannt“. Salz war stets ein wichtiges Handelsgut. Es fand sogar mehrfache Erwähnung in der Bibel.
Städte, die im Mittelalter über Salzlager verfügten waren in der Regel dadurch sehr reich. Viele Städte tragen deswegen das Wort „Salz“ (oder das keltische Wort „Hall“) auch im Namen (z.B. Halle, Reichenhall, Hallein, Halle, Schwäbisch Hall, Salzburg, Salzgitter, Bad Salzuffeln, Salzdettford, Bad Salzschlirf usw. München kam so zu Reichtum, da die Menschen eine Zollstation an der Isar bauten und gut an dem Salz aus Salzburg verdienten).
Menschen gewinnen Salz entweder durch Meerwasserentsalzung, Salzstöcke oder aus Solen. Dabei wird Wasser in den unterirdischen Salzstock gegeben, das Salz löst sich auf, das Wasser anschließend verdunstet und das Salz bleibt zurück.
Bei der Meerwasserverdunstung läuft Meerwasser dabei in einer speziell vorbereiteten Bucht von Becken zu Becken. Durch die Sonnenwärme wird das Meerwasser dabei verdampft. Zurück bleibt das feste Salz.
- In den Meeren und in unterirdischen Salzlagerstätten findet man vor allem das Salz Natriumchlorid. Wir verwenden es als Speisesalz.
- Ca. 90% der unterirdischen Salzlagerstätten sind durch eingetrocknete Meere entstanden. Der Rest befindet sich in z.B. in Binnenseen oder als Sediment (=Ablagerungsgestein) im Boden
- Der Salzgehalt des Meerwassers ist seit ca. 2 Milliarden Jahren ungefähr gleich.
- Je nach Gestein befinden sich aber in jedem Boden geringe Mengen an Salzen. Ein winziger Teil davon kann sich durch versickerndes Regenwasser auflösen, sodass dann das Grundwasser einen natürlichen Salzgehalt hat. Deshalb schmecken auch viele Mineralwasser unterschiedlich. Dabei hängt die Zusammensetzung des Salzes von den Salzen im Boden ab, in dem sich das Regenwasser gelöst hatte
- Nicht gesalzenes Wasser kann maximal 26% Kochsalz lösen. Für andere Salze gibt es andere Werte.
- Salze werden z.B. durch Regen aus dem Gestein gelöst und mit Flüssen dann ins Meer getragen. Deshalb entsprach der Salzgehalt des Meerwassers schon vor ca. 2 Mrd. dem heutigen.
Gebrauch und Verwendung von Salzen
-
Kochsalz wird vor allem zum Würzen verwendet: Viele Salze sind für menschliche Ernährung unentbehrlich (z.B. Kochsalz (=Natriumchlorid), Magnesium- und Calciumsalze usw.) Kochsalz wird zum Würzen von fast allen Speisen verwendet. Selbst im Brot ist es enthalten. Es ist für den Menschen lebenswichtig! Dabei sind beide Ionen, das Natriumion und das Chloridion biologisch für den Körper wichtig.
-
Neben geschmacklichen Gründen wird es bei Lebensmitteln auch zur Konservierung eingesetzt (Pökelfleisch, Fischkonservierung, etc.).
-
Jedes Jahr werden große Mengen an Streusalz im Winter verwendet. Es setzt den Schmelzpunkt von Wasser herab, sodass Schnee und Eis auf den Straßen schmelzen.
-
Natriumchlorid (Kochsalz) wird als Rohstoff in der chemischen Industrie häufig verwendet. So dient es z.B. der Chlorherstellung (Chlor dient als Ausgangsstoff der chemischen Industrie sowie der Bleich- und Desinfektionsmittelherstellung)
-
0,9%ige Natriumchloridlösung wird in der Medizin als physiologische Kochsalzlösung verwendet. Mit ihr kann man nicht nur Kontaktlinsen lagern, sondern auch Blut verdünnen oder Organe zur Transplantation lagern.
-
Soda (=Natriumcarbonat) neben der Herstellung von Limonade auch als Rohstoff für die Glasindustrie, zur Herstellung von Bleichmitteln, Farben, Füllstoffen sowie zur Entschwefelung von Roheisen, Gusseisen und Stahl verwendet (Soda =Natriumcarbonatdekahydrat (Na2CO3 · 10 H2O))
-
Salze sind als sogenannte „Tenside“ in Seifen und Waschmitteln unentbehrlich.
-
Einige Salze, wie z.B. Kochsalz, sind für die menschliche Ernährung unverzichtbar. Deshalb sind Salze wichtiger Bestandteil unserer Nahrung.
Zusammensetzung der Salze
Feste Salze sind Verbindungen, die aus positiven Metallkationen und negativen Säurerestanionen bestehen, die abwechselnd angeordnet sind. Diese Anordnung nennt man auch Ionengitter.
Im gelösten Zustand enthält die wässrige Lösung dann beide Ionensorten in freibeweglicher Form. Dieses kennzeichnet man durch ein „(aq)“ am Ion (z.B. Li+(aq)).
Der Schmelzpunkt von Salzen ist sehr hoch
In Salzen liegen also Ionen vor. Diese haben eine positive oder negative Ladung. Natriumchlorid besteht aus positiven Natriumionen und negativen Chloridionen. Positive und negative Ionen ziehen sich gegenseitig an. Besonders im Feststoff ist diese Anziehung besonders stark.
Aus dem Kapitel über die Eigenbewegung der Teilchen weißt Du schon, dass alle Teilchen schwingen. Also auch Ionen!
Was passiert nun beim Schmelzen eines Salzes?
Die Ionen beginnen zu schwingen und brechen dadurch den „Ionenverbund“ aus positiven und negativen Ionen auf.
=> Ionen werden frei beweglich, das Salz schmilzt.
Beim Schmelzen von Salzen werden dabei also die Ionen voneinander getrennt. Durch Zufügen von Energie erhöht sich dabei die Eigenschwingung der Ionen. Überschreitet die Energie den Schmelzpunkt, ist die Schwingung so groß, das der Verband aus Ionen „zusammenbricht“.
Insgesamt kann man sagen, dass bei Salzen der Schmelzpunkt sehr hoch ist, da die Ionen sich durch die Ionenladung gegenseitig zusammenhalten und man „mehr“ Wärmeenergie zufügen muss, um den Verbund zu lösen, als bei Verbindungen, die keine Ladungen enthalten (z.B. Zucker).
Bergmännische Gewinnung von Natriumchlorid

In Deutschland wird Kochsalz vor allem unter Tage abgebaut, da aufgrund des Klimas eine Meerwasserentsalzung nicht für ganz Deutschland ausreichen würde.
Die Hauptkorridore befinden sich viele hundert Meter unter dem Boden. Von diesen zweigen Seitenkorridore ab.

An der Decke erkennt man manchmal Verunreinigungen durch andere Salzschichten als Natriumchlorid. Typische Verunreinigungen sind Eisensalze, Kupfersalze und Bariumsalze.

Das Abbauprodukt: Steinsalz. Es enthält hauptsächlich Natriumchlorid, ist aber noch verunreinigt, wie man sieht.

Mit einem solchen Bohrer wird das relativ weiche Gestein gelöst und abgeschabt. Die Decke erhält dabei ihre typische Struktur.

Das gereinigte Produkt: Kochsalz
Aufgaben:
1. Wegen Salz wurden früher Kriege geführt. Es war mancherorts so wertvoll, dass es das weiße Gold genannt wurde.
Erstelle ein Video oder einen Text unter der Überschrift: „Die Bedeutung des Salzes“.
2. Bestimme die Ionenladungen der folgenden Ionen:
Na; Cl, Mg; Li; Sr; Be; S; O; Al, O; C; H; K; Ca; Ba; Br; I; F; Ne
3. Bestimme die richtige Formel für folgende Salze:
Natriumchlorid (= Kochsalz):
Bariumsulfat:
Magnesiumcarbonat:
Natriumsulfat:
Lithiumnitrat:
Kaliumbromid:
Calciumphosphat:
Aluminiumsulfat:
4. Fasse mit Deinen Worten zusammen, warum Salze eine so große Gruppe der Chemie darstellen.
Zusatzinformationen:
https://de.wikipedia.org/wiki/Salze
https://de.wikipedia.org/wiki/Natriumchlorid
Nomenklatur bei Salzen
Salze werden nach mit dem Atomnamen des Metallions und dem Säurerest benannt.
Zuerst wird dabei das Metallion genannt, dann der Säurerest.
Zum Beispiel: Natriumchlorid, Magnesiumsulfat usw.
Die Wertigkeit des Metallions (bzw. dessen Ionenladung) kann dabei durch eine griechische Zahl angegeben werden. Bsp.: Eisen-(III)-chlorid.
|
1 |
mono |
|
2 |
di |
|
3 |
tri |
|
4 |
tetra |
|
5 |
penta |
|
6 |
hexa |
|
7 |
hepta |
|
8 |
octa |
|
9 |
nona |
|
10 |
deca |
Übungen zu Salzformeln und Salznamen
1. Schreibe hinter jedes Symbol die passende Ionenladung und kombiniere anschließend die Ionen zu nach „außen“ hin ungeladenen Salzen. Schreibe unter die Salzformel den passenden Namen:
|
F |
Cl |
S |
O |
NO3 |
SO4 |
PO4 |
|
|
K |
|||||||
|
Li |
|||||||
|
Na |
|||||||
|
Ca |
|||||||
|
Al |
|||||||
|
Fe2+ |
|||||||
|
Fe3+ |
|||||||
|
Pb |
|||||||
|
Cr |
|||||||
|
Cu |
2. Vervollständige die Sätze:
-
Ionen entstehen durch...
-
Ionen unterschieden sich von Atomen durch...
-
Salze sind so aufgebaut, dass…
-
Ionen haben die Eigenschaften…
-
Ionenladungen bestimmt man…
-
Die Ladung eines Säurerestes kann man bestimmen, indem…
3. Welche Voraussetzungen müssen gegeben sein, damit Ionen den Strom leiten?
Übungstest zum Thema „Salze und Ionen“
1) Welche der folgenden Stoffe sind gute Leiter für elektrischen Strom? (je 0,5P => 4P)
-
Zuckerlösung Erklärung:
-
Magnesiumchloridlösung
-
Natriumsulfatkristall
-
Kochsalzschmelze
-
Silberchlorid in Wasser
-
Wasser aus der Leitung
-
Metallstab
-
Kohlenstoffdioxid
2) Definiere den Begriff „Ion“: (2P)
3) Welche Unterschiede bestehen zwischen Natrium als Element und dem Natriumion? (4P)
4) Unterstreiche bei den Begriffen Anionen in rot und Kationen in grün und notiere dann die entsprechende Formel mit ihrer Ionenladung. (Begriffe je Ion 0,25P + je Formel 0,25P => 6 P)
- Natriumion:
- Nitration:
- Sulfation:
- Carbonation:
- Berilliumion:
- Chloridion:
- Sulfidion:
- Fluoridion:
- Magnesiumion:
- Phosphation:
- Oxidion:
- Silberion:
5) Bestimme die Ionenladungen der Ionen und erstelle dann die Summenformel, welche sie im entsprechenden Salzkristall haben. Zum Schluss markiere die schwerlöslichen Salze (je 0,25P => 9P)
|
F |
Cl |
S |
SO4 |
CO3 |
PO4 |
|
|
K |
||||||
|
Li |
||||||
|
Ca |
||||||
|
Al |
||||||
|
Ba |
||||||
|
Ag |
6) Nenne die allgemeine Regel, nach der Salze aufgebaut sind und beschreibe dann die genaue Anordnung. Gehe dabei auch auf den vorliegenden Bindungstyp ein. (4P)
7) Wenn man in Trinkwasser Silbernitratlösung tropft, kommt es zu einer leichten Trübung.
Beschreibe die Reaktion genau und benenne den sich bildenden Stoff. (Rückseite) (6P)
Vier Möglichkeiten der Salzbildung
Salze lassen sich auf mehreren Wegen bilden. Diese sind auch in der Natur so zu finden.
I) Salzbildung durch Neutralisation
Diesen Weg kennst Du schon aus dem Kapitel „Neutralisation“.
V: Zu Schwefelsäure wird erst etwas Universalindikator und dann tropfenweise Kalilauge zugefügt. Die neutrale Lösung wird eingedampft.
B: Lösung wird warm, nach dem Eindampfen liegt ein weißer Feststoff vor.
Bsp.: H2SO4 + 2 KOH ---> K2SO4 + 2 H2O + E
Allgemeine Regel: Säure + Lauge ---> Salz + Wasser + E
II) Salzbildung aus Metalloxid und Säure
V1: a) Etwa 4 cm Magnesiumband wird mit einer Tiegelzange in die Bunsenbrennerflamme gehalten. Gib das Reaktionsprodukt in ein Reagenzglas. (Hinweis: Nicht in die Flamme schauen!)
b) Salzbildung: In das Reagenzglas wird verdünnte HCl gegeben (etwa 2cm hoch). Dampfe anschließend die Lösung ein. Benutze dabei unbedingt die Schutzbrille!
B: a) Mg verbrennt mit sehr heller Flamme. Das Reaktionsprodukt ist ein weißes Pulver.
b) Das Oxid löst sich in der Säure, beim Eindampfen erhält man einen farblosen Feststoff.
S: a) 2 Mg + O2 ---> 2 MgO (Magnesiumoxid)
b) MgO + 2 HCl ---> H2O+MgCl2 (Magnesiumchlorid)
Allgemeine Regel: Metalloxid + Säure ---> Salz + Wasser + E
III) Salzbildung aus Nichtmetalloxid und Lauge
Erinnere Dich an die Herstellung von frischem Kalkwasser:
a) Vorbereitung: Herstellung von frischem Kalkwasser
Überschichte 2 Spatelspitzen CaO mit Wasser und schüttle kräftig. Filtriere die entstandene Lösung.
CaO + H2O ---> Ca(OH)2 (Kalkwasser)
b) Salzbildung aus Nichtmetalloxid und Lauge
V: Kohlenstoffdioxid wird in Kalkwasser geleitet. Es bildet sich das schwerlösliche Salz Calciumcarbonat (=Kalk). Dazu wird mithilfe einer Pipette mehrmals ausgeatmete Luft in die Lösung von Kalkwasser geblasen.
B: Die Lösung färbt sich milchig-trüb.
S: Ca(OH)2 + CO2 ---> CaCO3 + H2O + E
Calciumcarbonat (Salz)
Calciumcarbonat (Kalk) ist ein schwerlösliches Salz. Es löst sich nur in geringem Maße2.
Allgemeine Regel: Nichtmetalloxid + Lauge ---> Salz + Wasser + E
Anmerkung: Im Grunde entsprechen die Wege 2. und 3. dem ersten, da in Nichtmetalloxide mit Wasser Säuren bildet und Metalloxide mit Wasser Laugen entstehen lassen.
IV) Salzbildung aus den Elementen
V: ca. 5g Magnesium (alternativ Zink) werden mit ca. 3g Iod (I2) vorsichtig vermischt. Das fertige Gemisch wird dann auf ein Uhrgläschen gebracht und im Abzug vorsichtig mit wenigen Tropfen Wasser aus der Spritzflasche benetzt.
Alternativ kann der Versuch im Reagenzglas durchgeführt werden. Dann kann nach Reaktionsende deutlich mehr Wasser zugefügt werden, in dem sich das Salz löst. Das Wasser wird abdekantiert und anschließend eingedampft.

Je eine Spatelspitze Mg und I2 und dann Schütteln!
B: Heftige Reaktion, Bildung eines hellen Feststoffs, violette Ioddämpfe. Der Feststoff löst sich in Wasser. Nach dem Eindampfen der Lösung ist er am Reagenzglasboden sichtbar.
S: Bei der Reaktion von Mg und I2 entsteht (festes) Magnesiumchlorid. Dieses ist aus Ionen aufgebaut (Salz!) => Bei der Reaktion hat ein Magnesiumatom Elektronen an 2 Iodatome abgegeben:
S: Es ist das Salz Magnesiumiodid entstanden
Mg ---> Mg2+ + 2 e–
I2 + 2 e– ---> 2 I–
————————————————
Mg + I2 ---> Mg2+I–2 + E
Allgemeine Regel: Metall + Nichtmetall ---> Salz
Zusammenfassung: Salzbildung
Salzbildung: Salze können durch verschiedene Reaktionen entstehen. Dabei meint man immer eine chemische Reaktion, bei der am Ende ein Salz vorliegt.
Nicht verwechseln: Die „Salzgewinnung“ hingegen ist nicht der chemische Vorgang, sondern der Abbau durch den Menschen.
Salzbildung durch Reaktion von Säure und Lauge
HCl + NaOH ---> NaCl + H2O
Salzbildung durch Reaktion von Metalloxid und Säure
CaO + H2O ---> Ca(OH)2
Salzbildung durch Reaktion von Nichtmetalloxid und Lauge
Ca(OH)2 + CO2 ---> CaCO3 + H2O + E
Salzbildung aus den Elementen
Mg + I2 ---> MgI2
Salzbildung aus Metallen und Säuren
Mg + 2HCl ---> MgCl2 + H2
Aufgaben zur Salzbildung
1. Vervollständige die Gleichungen:
Metalloxid + Säure:
Calciumoxid + Salzsäure
CaO + __HCl ---> +
Calciumoxid + Phosphorsäure
CaO + __H3PO4 ---> +
Nichtmetalloxid + Lauge:
Schwefeldioxid + Barytwasser
SO2 + Ba(OH)2 ---> +
Kohlendioxid + Natronlauge
CO2 + __NaOH ---> +
2. Metall + Nichtmetall:
Magnesium + Brom
Mg + Br2 --->
Eisen + Chlor (es entsteht Eisen(III)-chlorid)
__ Fe + __ Cl2 --->
2. Stelle drei allgemeine Regeln auf, wie Salze entstehen können. Verfahre nach dem Muster „reagieren Oxide mit ... , entstehen Salze“.
3. Erkläre die Besonderheit der Edelgase und die Edelgaskonfiguration.
4. Wenn Du eine Energiebetrachtung zu allen Salzbildungen durchführst, was fällt dann auf?
Salzbildung II: Die Bildung von Zinksulfid aus den Elementen
V: Zur Vereinigung von Zink und Schwefel werden beide Elemente miteinander vermischt und auf einem Drahtnetz mit einem glühenden Draht entzündet.
glühender Metallstab entzündet das Gemisch
(Zink und Schwefelpulver vermischt (2:1))

B: Sehr heftige Reaktion, Rauchentwicklung
S: Es fand eine Salzbildung statt. Die Reaktion ist stark exotherm. Der neue Stoff heißt Zinksulfid.
Zum Aufstellen der Reaktionsgleichung muss man wissen, dass Zn zwei Valenzelektronen besitzt:
Zn ---> Zn2+ + 2 e–
S + 2 e– ---> S2–
———————————————
Zn + S ---> Zn2+ S2– + E
Unterkapitel III: Der Aufbau von Salzkristallen und energetische Aspekte der Salz- und Ionenbildung
Salze im festen Zustand: Der Aufbau der Salzkristalle - das Ionengitter
Ansetzten eine Kristallzucht:
V: Eine Kupfersulfatlösung wird übersättigt. Anschließend wird ein Faden mit einem Impfkristall hineingehängt.
B: Es bildet ein Salzkristall.
S: Die ursprünglich frei beweglichen Ionen ziehen sich gegenseitig an und bilden einen Ionenverband bei dem sich die Kationen und die Anionen gegenseitig anziehen.
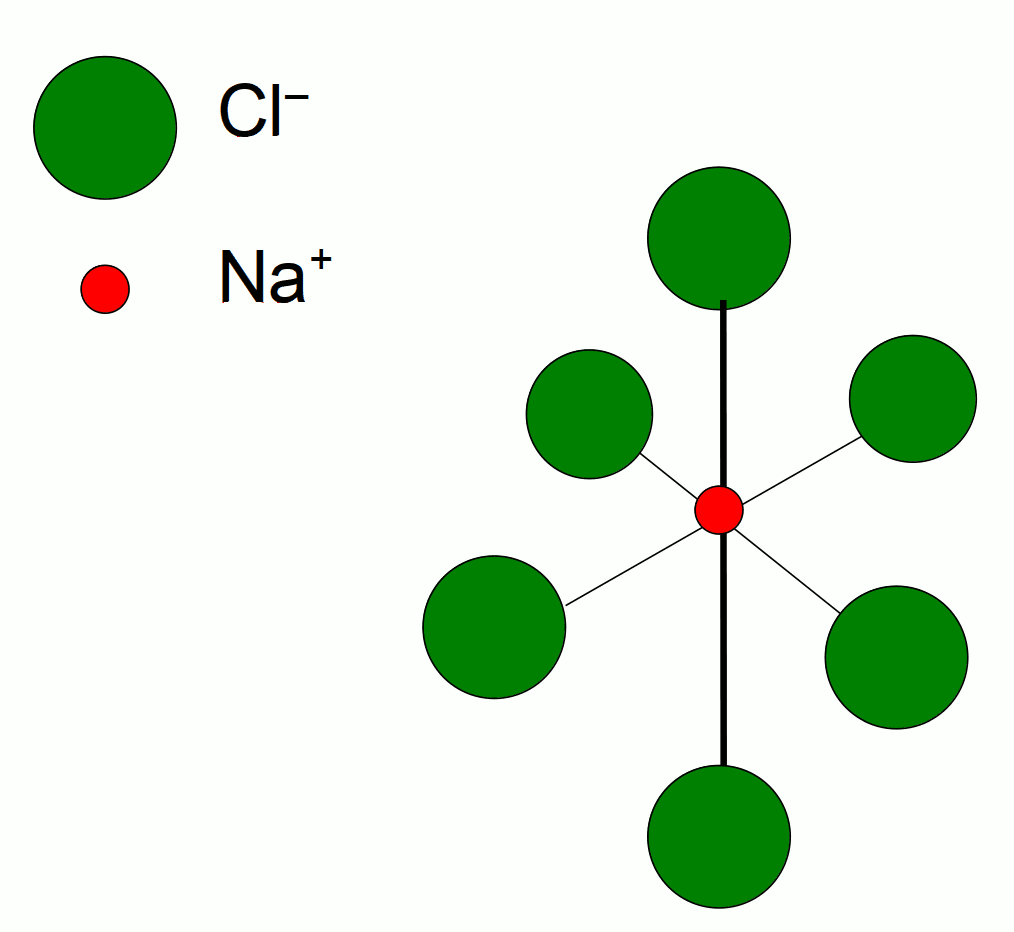
Elementarzelle NaCl, Koordinationszahl 6
Die Verbindung der positiv und negativ geladenen Ionen zu einem stabilen Verband/ Gitter setzt eine hohe Gitterenergie frei (es ist also ein stark exothermer Schritt). Sie beruht auf der starken Anziehungskraft zwischen den Ionen entgegengesetzter Ladung.
Max von Laue - Versuch
Max von Laue war Physiker, der an der Universität Straßburg studierte und sich dann später, nach seinem Umzug nach Göttingen schwerpunktmäßig mit Optik beschäftigte. 1903 promovierte er bei Max Planck in Berlin. Nach seiner Habilitation 1906 beschäftigte er sich als Professor mit der Relativitätstheorie Albert Einsteins und entwickelte 1907 mit seinen optischen Experimenten wichtige Beweise für die Richtigkeit des Einsteinschen Additionstheorems. 1909 kam er als Privatdozent an das Institut für theoretische Physik der Universität München. Er war Spezialist für Licht und Strahlung und erkannte viele Gemeinsamkeiten mit den radioaktiven Strahlen.
Im Jahr 1912 entdeckte er zusammen mit Friedrich und Knipping die Beugung von Röntgenstrahlen an Kristallen. Damit waren sowohl der Wellencharakter der Röntgenstrahlung als auch die Gitterstruktur der Kristalle nachgewiesen. Für seine Arbeit erhielt Max von Laue 1914 den Nobelpreis für Physik.
Der Laue-Versuch:
V: Ein Salzkristall wird mit Röntgenstrahlung bestrahlt. Dahinter befindet sich eine Fotoplatte, welche für Röntgenstrahlen empfindlich ist3.
B: Laue bemerkte charakteristische Schwärzungen. Er untersuchte daraufhin verschiedene Salze und stelle fest, dass es scheinbar drei Typen von Mustern gab, die besonders häufig auftreten.
Ergebnis des Max von Laue Versuchs
S: Im festen Zustand liegt in Salze ein Ionengitter vor. Dabei sind Ionen im richtigen stöchiometrischen Verhältnis so „gepackt“, dass jedes Kation die gleiche Anzahl an Anionen als Nachbarn hat (und umgekehrt). Ein positives Ion hat also nur negative Ionen als Nachbar und umgekehrt. Die Anzahl ist dabei immer gleich! Diese Zahl nannte er Koordinationszahl. Die Koordinationszahl gibt die Anzahl der unmittelbaren Nachbarn an, welche für die jeweiligen Salze typisch ist!
Es gibt dabei v.a. drei wichtige Typen, die besonders häufig auftreten. Laue benannte sie nach den Salzen, wo er dies zuerst bemerkte:
NaCl: Natriumchlorid-Typ KZ = 6 (also 6 Nachbarn pro Ion) bildet einen Oktaeder.
CsCl: Cäsiumchlorid-Typ KZ = 8 (also 8 Nachbarn pro Ion) bildet einen Würfel.
ZnS: Zinksulfid-Typ KZ = 4 (also nur 4 Nachbarn pro Ion) bildet einen Tetraeder.
Aber warum ist die Summenformel dann NaCl?
Wenn aber jedes Ion so viele Nachbarn hat, warum ist dann die Summenformel nicht NaxClx?
Das wäre doch viel zu chaotisch und kompliziert!
Die Summenformel gibt also nur das Verhältnis der Ionen an.
Bsp.: Na+Cl– : Verhältnis Na+ : Cl– = 1:1
Zusatzinformationen:
https://de.wikipedia.org/wiki/Max_von_Laue
Die Anziehungskraft der Ionen
Aus dem Versuch der Natriumchloridbildung weißt Du schon, dass die Ionengitterbildung ein exothermer Prozess ist. Diese Energie wurde frei, da sich anziehende (unterschiedlich geladene) Teilchen aufeinandertreffen.
Versucht man nun, zwei miteinander verbundene Ionen voneinander zu trennen, benötigt man Energie. Dies kann man im täglichen Leben gut durch das Auseinanderziehen zweier Magneten verdeutlichen:
Zwei miteinander verbundene Teilchen kann man nur durch das Aufbringen von Energie voneinander trennen!
Man kann sogar berechnen, wie groß die Energie ist, die bei der Gitterbildung frei wird, bzw. die aufgebracht werden muss, um das Gitter zu zerstören (schmelzen)4. Diese Energie entspricht im Betrag dem Energiebetrag, der notwendig ist, die Ionen wieder voneinander zu trennen.
Die Koordinationszahl
Die Anordnung der Ionen im Kristall ist regelmäßig. Betrachtet man z.B. einen Natriumchloridkristall, sieht man:
-
Jedes Na+-Ion ist von 6 Cl–-Ionen umgeben.
-
Jedes Cl–-Ion ist von 6 Na+-Ionen umgeben.
=> Man sagt daher die Koordinationszahl (KZ) beim Kochsalz ist 6.
Die Koordinationszahl ist die Anzahl der direkten Nachbarn in einem
regelmäßig aufgebauten Verband.
Beispiele für Koordinationszahlen der Ionengitter
NaCl KZ = 6
CsCl KZ = 8
ZnS KZ = 4
Diese drei Typen stehen exemplarisch ebenfalls für viele andere Salze. Verbinden sich also Ionen mit der Koordinationszahl 6, spricht man vom NaCl-Typ, bei KZ 8 vom CsCl-Typ und bei KZ 4 vom ZnS-Typ.
Wovon hängt die Koordinationszahl ab?
1) Vom Ionenradius: Je größer ein Anion ist, desto mehr Kationen könnten darum angeordnet werden.
2) Die Formel gibt an, wie sich die Zahlen von Anionen und Kationen in der Verbindung zueinander verhalten.
Die Formel einer Ionenverbindung ist immer eine Verhältnisformel, keine Molekülformel
Beispiele für Ionenradien:
|
r(Na+) |
r(Cs+) |
r(Zn2+) |
r(Cl-) |
r(S2-) |
|
|
97 pm |
169 pm |
74 pm |
181 pm |
184 pm |
|
rKation/ rAnion |
Koordinations- zahl
|
Anordnung der Ionen |
Gittertyp |
|
< 0,42 |
4 |
tetraedrisch |
ZnS-Typ |
|
0,42 bis 0,73 |
6 |
oktaedrisch |
NaCl-Typ |
|
> 0,73 |
8 |
würfelförmig |
CsCl-Typ |
Aufgaben:
Ermittle die Koordinationszahlen den und Gittertyp von Lithiumbromid: r(Li+) = 68 pm, r(Br-) = 195 pm
Wovon hängt der Ionenradius ab?
Zwei Faktoren beeinflussen den Ionenradius:
a) Die Anzahl an Elektronenhüllen:
Von Periode zu Periode nehmen die Ionenradien zu, da mit jeder Periode auch eine neue Elektronenhülle (Schale) vorhanden ist => der Radius nimmt zu!
b) Die Anzahl an Valenzelektronen:
Werden Elektronen abgegeben, so wird die Edelgaskonfiguration der darunterliegenden Hülle (Schale) erreicht. Es entstehen positiv geladene Ionen (Kationen). Es gilt also folgende Regel: Kationen sind kleiner als die Anionen derselben Periode.
Schaut man aber innerhalb einer Elektronenhülle, dann nimmt der Radios mit steigender Ordnungszahl leicht ab, da immer mehr Protonen im Kern vorhanden sind.
Erklärung: Von Element zu Element nimmt innerhalb einer Periode die Kernladungszahl (= Protonenzahl) zu. Das heißt, die Außenelektronen werden immer stärker durch mehr und mehr Protonen angezogen.
=> Der Radius nimmt leicht ab.
Grobe Faustregel: Bei der Kationenbildung nimmt der Ionenradius ab, bei der Anionenbildung hingegen nur unmerklich zu
Von der Größe der Ionen ist im Übrigen auch die Anzahl an Nachbarn im Salzkristall abhängig (=Koordinationszahl). Sie bestimmt u.a. auch die Form der Salzkristalle.
Vergleiche Atomradios und Ionenradius:
-
Bei Kationen, also positiv geladenen Ionen, ist der Ionenradius kleiner als der Atomradius. Je größer die positive Ladung ist, desto kleiner wird der Ionenradius.
-
Bei Anionen, also negativ geladenen Ionen, ist der Ionenradius größer als der Atomradius. Je größer die negative Ladung ist, desto größer wird der Ionenradius.
Zusatzinformationen:
https://de.wikipedia.org/wiki/Coulombsches_Gesetz
Die wichtigsten Atom- und Ionenradien
Vergleiche einmal Ionenradien und die jeweilig entsprechenden Atomradien. Kannst Du eine generelle Aussage treffen, die zwischen Anionen und Kationen unterscheidet?
|
Atomradius |
Ionenradius |
|
|
Ag |
144 |
Ag+: 115 |
|
Al |
143 |
Al3+: 57 |
|
Ba |
217 |
Ba2+: 143 |
|
Be |
111 |
Be2+: 34 |
|
Br |
114 |
Br–: 196 |
|
Ca |
197 |
Ca2+: 106 |
|
Cl |
99 |
Cl-: 181 |
|
F |
64 |
F –: 133 |
|
Fe |
124 |
Fe3+: 67 |
|
H |
30 |
H–: 154 |
|
I |
133 |
I–: 220 |
|
K |
227 |
K+: 133 |
|
Li |
152 |
Li+: 60 |
|
Mg |
160 |
Mg2+: 78 |
|
Mn |
137 |
Mn2+: 91 |
|
N |
70 |
N3–: 171 |
|
Na |
186 |
Na+: 98 |
|
O |
66 |
O2–: 132 |
|
P |
110 |
P3–: 212 |
|
Pb |
175 |
Pb2+: 132 |
|
S |
104 |
S2–: 195 |
Ionosierungsenergien
Schaut man sich den Vorgang der Ionenbildung aus den jeweiligen Elementen genauer an, so sieht man, dass die Abgabe bzw. die Aufnahme eines Elektrons Energie benötigt. Um das genau zu verstehen, müssen wir uns ein wenig erinnern:
Erinnere Dich:
|
Na |
Mg |
Al |
Si |
P |
S |
Cl |
Ar |
|
<-------- Metalle ------> |
Halbmetall |
<-------- Nichtmetalle ------> |
|||||
-
Innerhalb einer Hauptgruppe sind die Eigenschaften der Elemente teilweise sehr ähnlich.
-
Innerhalb einer Periode folgen Elemente mit sehr unterschiedlichen Eigenschaften aufeinander.
-
In einer Periode nimmt von links nach rechts die Ordnungszahl und damit auch die Elektronenzahl und die Kernladungszahl (letzteres durch die Zunahme an Protonen) um jeweils eine Einheit zu.
-
Da chemische Eigenschaften vor allem durch die Zahl der Valenzelektronen bestimmt sind, unterscheiden sich Elemente innerhalb einer Periode erheblich in ihren chemischen Eigenschaften.
-
Im PSE werden die Elemente nach steigender Ordnungszahl (Kernladungszahl) geordnet.
-
Je mehr Protonen nun im Kern sind, desto mehr nimmt die Anziehung zwischen Kern und Elektronenhülle zu und es wird folglich immer schwerer, Valenzelektronen abzuspalten (Kationen-Bildung) und immer leichter Elektronen aufzunehmen (Anionen-Bildung). Je leichter es ist, desto weniger Energie wird benötigt. Je schwerer es ist, desto mehr Energie wird benötigt.
-
Die Zugabe oder Wegnahme eines Elektrons ist dabei immer „preiswerter“, es wird also weniger Energie benötigt, als für die Abgabe oder Zugabe von einem zweiten, dritten oder gar vierten Elektron notwendig wäre. Deshalb gibt es auch so wenige Ionen mit hohen Ionenladungen.
1. Ionisierungsenergie
-
Elektronenaffinität
-
Atomradius
|
Ionisierungsenergie [eV] |
|
|
C ---> C+ |
11,3 |
|
C+ ---> C2+ |
24,4 |
|
C2+ ---> C3+ |
47,9 |
|
C3+ ---> C4+ |
64,5 |
|
C4+ ---> C5+ |
392 |
Merke: Die Periodennummer gibt die Zahl der Elektronenschalen/ Elektonenhüllen an.
Die Hauptgruppennummer gibt die Zahl der Valenzelektronen an.
Ionenbindung und das Ionengitter
Def.: Eine Ionenbindung ist die Verbindung von unterschiedlich geladenen Ionen.
Die Ionen ziehen sich dabei durch elektrostatische Anziehung an und „halten“ so zusammen. Diese Ionenbindung kann z.B. durch einen Elektronenübergang von einem Atom auf ein Zweites entstehen (z.B. bei der Salzbildung). Dabei werden jeweils soviel Elektronen aufgenommen (bzw. abgegeben), bis beide Partner Edelgaskonfiguration erreichen.
Regeln:
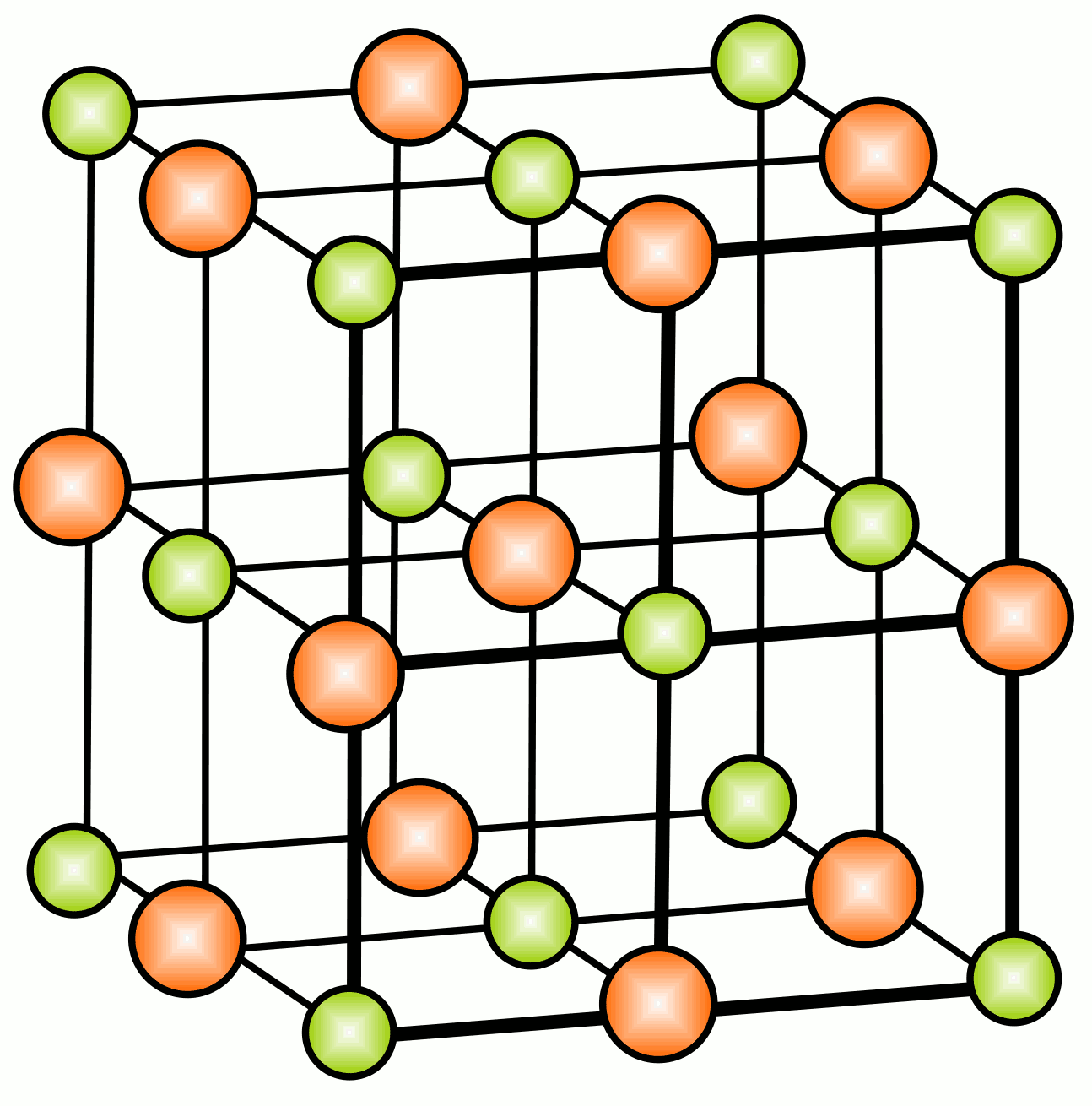
NaCl-Ionengitter (Ausschnitt)
-
Ein Ion kann aus einem oder mehreren Atomen bestehen (Na+, Cl–, NO3–).
-
Metallatome bilden Kationen. Diese sind positiv geladen und kleiner als das entsprechende Metallatom, da in ihrer Elektronenwolke ein Elektron fehlt. Nichtmetallatome bilden Anionen. Sie sind negativ geladen und ungefähr so groß wie das ursprüngliche Atom, da sich die Anzahl ihrer Elektronenwolken nicht ändert.
Chlor ---> Chlorid (Cl–) Schwefel ---> Sulfid (S2–) -
Eine aus Ionen aufgebaute Verbindung besteht aus zahlreichen Anionen und
Kationen, die im festen Zustand zu einem Ionengitter (Kristall) geordnet sind.
Die elektrostatische Anziehung hält den Kristall zusammen. -
Die Koordinationszahl gibt die Zahl der unmittelbaren Nachbarn an.
(Bsp. NaCl: KZ = 6) -
Die Formel (z.B.: NaCl) gibt das einfachste ganzzahlige Verhältnis zwischen den
Ionen an. Insgesamt ist der Kristall elektrisch neutral. -
Bei der Bildung eines Ionengitters wird GITTERENERGIE frei. Das Ionengitter ist demnach ein von den Ionen „angestrebter“ Zustand. (Man glaubt es kaum, aber der geordnete Zustand ist der, der am wenigsten Energie benötigt)
-
Zum Auflösen eines Ionengitters wird demzufolge wieder der Betrag Gitterenergie benötigt, der bei der Bildung frei wurde (Um also „Unordnung“ zu erzeugen, muss Energie „reingesteckt“ werden.).
-
Beim Schmelzen von Salzen werden die Ionen des Ionengitters voneinander getrennt. Durch Zufügen von Energie erhöht sich dabei die Eigenschwingung der Ionen. Überschreitet die Energie den Schmelzpunkt (= Betrag der Gitterenergie), ist die Schwingung so groß, dass das Ionengitter „zusammenbricht“.
=> Da die Ionen sich durch die Ionenladung gegenseitig zusammenhalten, muss sehr viel Energie aufgebracht werden, um das Ionengitter zu zerstören.
=> Bei Salzen ist der Schmelzpunkt also sehr hoch!
Bei der Bildung eines Ions aus einem Atom wird Energie benötigt5:
Ionisierungsenergie (ΔHI): Energie, die benötigt wird, um aus einer Elektronenwolke eines Atoms ein Elektron zu entfernen.
Elektronenaffinität (ΔHEA): Energie, die benötigt bzw. frei wird, um einem Atom ein Elektron zuzufügen
Energiebilanz der Salzbildung
Die Salzbildung ist immer exotherm. Eine besonders exotherme Reaktion ist die Bildung von Natriumchlorid:
V: Reaktion von Natrium und Chlor.
B: Es entsteht ein weißer Feststoff. Die Reaktion ist stark exotherm.
S: Es ist Natriumchlorid entstanden. Große Energiemengen wurden frei.
Na ---> Na+ + e–
Cl2 + 2 e– ---> 2 Cl–
————————————————
2 Na + Cl2 ---> 2 NaCl + E
Teilschritte der NaCl - Bildung
Die Bildung von NaCl läuft in mehreren Schritten ab. Um die Heftigkeit der Reaktion besser zu verstehen, zerlegen wir sie mal in Einzelschritte:
Welche Teilschritte müssen ablaufen, damit Natrium und Chlor zu Natriumchlorid reagieren?
1a) Na ---> Na+
(1) Sublimation: (festes) Natrium (s) wird zu (gasförmigem) Natrium (g).
Dazu wird Energie benötigt => Sublimationsenergie ist endotherm >0
(2) Ionisierung: Natrium (g) wird unter Elektronenabgabe zum Na+-Ion.
Dazu wird Energie benötigt => Ionisierungsenergie ist endotherm >0
1b) ½ Cl2 ---> Cl–
(1) Dissoziation: Chlor wird in zwei Atome gespalten (Cl2 ---> Cl + Cl).
Dazu wird Energie benötigt => Dissoziationsenergie ist endotherm >0
(2) Elektronenaffinität: Das Chloratom wird unter Elektronenaufnahme zum Chloridion.
Dabei wird Energie frei => Elektronenaffinitätenergie ist exotherm <0
2) Gitterbildung
Die Vereinigung der gasförmigen Ionen zum Salzkristall ist stark exotherm! <0
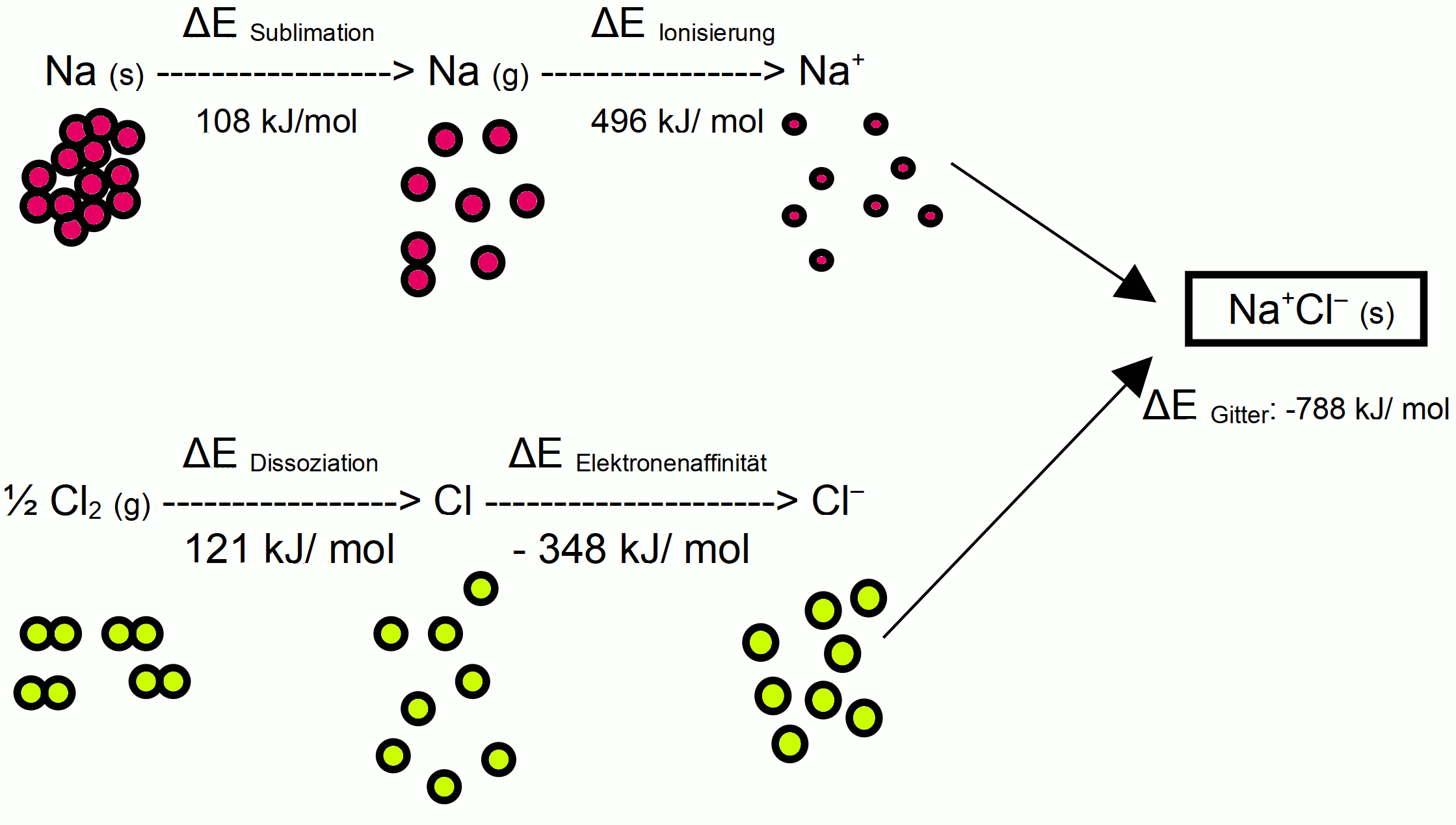
Gitterbildung mit beteiligeten Einergien bei NaCl
ΔESublimation ΔEIonisierung
Na (s) ---------------------> Na (g) --------------------> Na+
108 kJ/mol 496 kJ/ mol
ΔEDissoziation ΔEElektronenaffinität
½ Cl2 (g) -----------------------> Cl ---------------------------> Cl–
121 kJ/mol - 348 kJ/ mol

NaCl-Kristall
Die Verbindung der Ionen zu einem stabilen Verband/ Gitter setzt eine hohe Gitterenergie frei.
Die freiwerdende Gitterenergie beruht auf der starken Anziehungskraft zwischen den entgegengesetzt geladenen Ionen. Die „Triebkraft“ der Salzbildung ist also hohe freiwerdende Gitterenergie nicht das Erreichen des Edelgaszustandes6.
Den Zusammenhang kann man sich durch folgende Anschauung verdeutlichen. Um zwei Magneten zu trennen, benötigt man Energie. Fügt man sie wieder zusammen, wird genau diese Energie wieder frei.
Beachte das Vorzeichen der beteiligten Energien:
Sublimation: Endothermer Schritt, da ein fester Zusammenhalt gelöste werden muss
Ionisierung : Endothermer Schritt, da dem Natriumatom ein Elektron „genommen“ wird
(Ionisierungsenergie: Energie, die zum Ablösen eines Elektrons benötigt wird)
Dissoziation: Endothermer Schritt, da die beiden Atome des Moleküls „getrennt“ werden
Elektronenaufnahme: Exothermer Schritt, da Elektronen zugefügt werden.
Ist eigentlich logisch, denn wenn die Ionisierung endotherm ist, dann muss der gegenteilige Prozess exotherm sein!
(Die Elektronenaffinität ist die Energie, die bei der Aufnahme eines e- frei wird)
Gesamtbildungsenergie
Na (s) ---> Na (g) ΔHS = + 109 kJ/mol
Na (g) ---> Na+ + e- ΔHI = + 502 kJ/mol
½ Cl2 ---> Cl ΔHB = + 121 kJ/mol
Cl + e– ---> Cl- ΔHEA = - 365 kJ/mol
Na+ + Cl– ---> Na+Cl- ΔHG = - 778 kJ/mol
————————————————————————
Na + ½ Cl2 ---> Na+Cl- (s) ΔHR = - 411 kJ/mol
Berechnung der Bildungsenergie von NaCl:
ΔEBildung = ΔESubl + ΔEIonisierung + ½ ΔEDissoziation + ΔEElektronenaffinität + ΔEGitter
Das Erreichen der Edelgaskonfiguration kann somit nicht der Grund für die exotherm verlaufende Reaktion von Natrium und Chlor zum stabilen Natriumchlorid sein.
Vielmehr ist es das Zusammentreten der Ionen zu einem energiearmen, stabilen Gitter unter Freisetzung eines hohen Betrages an Gitterenergie. Die Edelgasregel ist somit ein geeignetes Hilfsmittel bei der Aufstellung der an der Salzbildung beteiligten Ionen, begründet jedoch nicht die „Triebkraft“ der Salzbildung.
Größe der Gitterenergie
Die Gitterenergie ist umso größer, je kleiner die Ionen und je höher deren Ladung ist.
Aufgaben:
-
Die Gitterenthalpien für die vier Lithiumsalze LiF, LiCl, LiBr und LiI betragen: -1036, -853, -807, -757 kJ/mol. Welche Schlüsse lassen sich daraus auf die Größe der Fluorid-, Chlorid-, Bromid- und IodidIonen ziehen? Begründe deine Antwort!
-
Magnesium, Calcium und Barium bilden als Elemente der 2. Hauptgruppe zweifach positiv geladene Ionen. Der Radius dieser Ionen steigt von 55 pm (Mg2+) über 99 pm (Ca2+) auf 135 pm (Ba2+).
Die Oxide dieser drei Metalle schmelzen bei 1920, 2570 bzw. 2800 oC.
Ordne diese Schmelzpunkte den drei Verbindungen zu! -
Berechne die Bildungsenergie für CsCl.
Cäsium:
ΔEsub = 78 kJ/ mol
ΔEion = 377 kJ/ mol Summe: 455 kJ/ mol
Chlor:
ΔEdiss = 242 kJ/ mol => E ½ Cl2 = 121 kJ/ mol
ΔEelektroaff = - 365 kJ/ mol Summe: -210 kJ/ mol
ΔEGitter = - 661 kJ/ mol
ΔE Bildung = - 450 kJ/ mol
Kalium:
ΔEsub = 90 kJ/mol
ΔEion = 425 kJ/mol
ΔER = - 439 kJ/ mol
Die Bildung von Zinksulfid in Teilschritten
1. Die Bildung von Atomen
Zn (fest, Atomverband) ---> Zn (g) Sublimationsenthalpie (> 0)
S (fest, Atomverband) ---> S (g) Sublimationsenthalpie (> 0)
2. Die Bildung von Ionen
Zn ---> Zn2+ + 2 e– Ionisierungsenergie (< 0)
S + 2 e– ---> S2– Elektronenaffinität (> 0)
3. Die Bildung des Ionengitters
Zn2+ + S2– ---> Zn2+S2– Gitterenergie (<< 0!)
Umkehrung der Salzbildung: Elektrolyse einer (wässrigen) Kupferchloridlösung
Eine Elektrolyse ist eine Aufspaltung einer Verbindung mithilfe von elektrischem Strom. Viele Elektrolysen sind in der Technik sehr wichtig: Die reine Form der Metalle Aluminium und Magnesium können nur elektrolytisch hergestellt werden.
V: In diesem Versuch soll durch Elektrizität Kupferchlorid gespalten werden. Eines der Produkte ist dabei sehr nützlich! Dazu werden in eine Kupferchloridlösung zwei Kohlenstoffelektroden getaucht und eine Spannung von 5V angelegt. Um den Versuch etwas zu verbessern, kann etwas Ammoniak zugefügt werden.

Elektrolyse von Kupferclorid (Kupferbildung)
B: Am Minuspol entsteht ein dunkelbrauner Feststoff.
Am Pluspol entsteht ein stechend riechendes Gas.
S:
Minuspol => Kathode: Kupferabscheidung
Pluspol => Anode: Chlorentwicklung
Detailzeichnung:

Elektrolyse zur Kupferpildung - Detailvorgänge bei der Elementbildung aus den Ionen
Die Elektrolyse ist eine chemische Reaktion, die erst durch das Zufügen von elektrischem Strom möglich wird. Dabei „liefert“ die Spannungsquelle Elektronen zum Minuspol, wodurch Kationen entladen werden.
Es entsteht (rotes) elementares Kupfer!
Am Pluspol „saugt“ die Spannungsquelle Elektronen von den Anionen ab, sodass auch diese entladen werden. Es bildet sich elementares Chlor! (die Spannungsquelle kann als „Elektronenpumpe“ gesehen werden).
- Pol (Anode):
1. Schritt: Cl– ---> [Cl] + e–
2. Schritt: 2[Cl] ---> Cl2
=> 2 Cl– ---> Cl2 + 2e–
+ Pol (Kathode): Cu2+ + 2e– ---> Cu
Gesamtreaktionsgleichung: 2Cl– + Cu2+ +E ---> Cl2 + Cu
Kathode: Kupferionen (= Kationen) + Elektronen ---> Kupferatome
Anode: Chloridionen (= Anionen) ---> Chloratome + Elektronen
(---> Chlormoleküle)
Verkupfern eines Schlüssels
Ein Schlüssel wird als Minuspol in einer Elektrolyse verwendet. Dabei ist ein dichter und geschlossener Kupferüberzug ist wünschenswert, da er stabiler und schöner ist. Fett von Fingern würde stören, also
ist vorher eine Entfettung, also eine Reinigung mit Spiritus (Alkohol) notwendig.
V: Elektrolyse einer Kupferionenlösung:

Skizze zur Verkupferung eines Metallschlüssels durch Elektrolyse
B: Am Schlüssel setzt sich schon nach kurzer Zeit ein rotbrauner Belag ab, der Anfangs schwarz erscheint.
=> An der Anode (Minuspol) entsteht ein dunkelbrauner Feststoff.
An der Kathode (Pluspol) entsteht ein stechend riechendes Gas.
S: Kupferchloridlösung enthalt Cu2+ und Cl─ Ionen. Legt man nun Gleichspannung an, so wandern diese Ionen zu ihren entgegengesetzten Polen, da ungleiche Ladungen sich anziehen. Kupferionen wandern also zum Minuspol (dem Metallschlüssel). Die Chloridionen wandern zum Pluspool.
Der Minuspol enthält durch die Spannungsquelle viele Elektronen, diese befinden sich im Schlüssel, wo sich bereits die ganzen Cu2+-Ionen angelagert haben. Diese Ionen nehmen nun die Elektronen auf und es entsteht elementares Kupfer:
Cu2+ + 2e─ ---> Cu
Aus den blauen Kupferionen entsteht also das Element, das Metall Kupfer, welches eine rotbraune Farbe hat).
Am Pluspol herrscht Elektronenmangel. Immer zwei Chloridionen geben dort jeweils ein Elektron ab und reagieren zusammen zum gasförmigen Element Chlor (das sind die Bläschen, die man sieht):
2Cl─ ---> Cl2 + 2e─
Gesamtreaktionsgleichung: 2Cl─ + Cu2+ ---> Cl2 + Cu
Als Verkupfern bezeichnet man das Überziehen metallischer Gegenstände mit Kupfer. Der Vorgang ist eine Sonderform der Elektrolyse.
Allerdings steht nicht die Zersetzung des Salzes im Vordergrund, sondern vielmehr das entstehende Produkt Kupfer. Bei geeigneten Bedingungen legt es sich auf dem metallischen Gegenstand, der als Minuspol dient ab.
Das Video zum Versuch: https://youtu.be/IqpSPAITs2g
Anwendungen der Elektrolyse
Die Elektrolyse ist ein Verfahren mit dem man Metalle mit einem anderen, edlerem Metall überziehen kann (z.B. Kupfer, Zink, Chrom).
Sie ist aber auch das wichtigste Verfahren um unedle metalle, welche im Boden nur als Salz vorkommen in Elemente umzuwandeln.
Ein Beispiel dafür ist die Gewinnung von Aluminium aus Aluminiumoxid:
2Al2O3 ---> 4 Al + 3O2
Aufgaben:
1. Stelle die Reaktionsgleichung einer Magnesiumchloridlösung Elektrolyse auf. Welche Produkte entstehen?
Tipps für eine dauerhaft haltende Kupferschicht bei der Verkupferung
-
Damit die Kupferschicht gut hält, ist es am besten, wenn man einen Kupferkomplex bildet. Dazu wird Kupfer in Drahtform in Ammoniumnitratlösung gelegt. Nach einigen Tagen ist die Lösung tiefblau. Dabei bildet sich der Kupfertetramminkomplex [Cu(NH3)4]2+.
-
Den Schlüssel nicht zu lang im Kupferbad lassen. Geeignet sind zum Beispiel bei 5V und ca. 8-9Amp 30 Sekunden Reaktionszeit.
-
Den Schlüssel vorher gut entfetten. Dies gelingt sowohl mit Spiritus, Nitroverdünner oder Aceton.
Zusatzinformationen:
Andere Möglichkeiten zum Verkupfern: https://de.wikipedia.org/wiki/Verkupfern
https://de.wikipedia.org/wiki/Elektrolyse
Ionenkristalltypen im Detail (nur für den LK)
Kristallisiert eine Salzlösung aus, bildet sich automatisch ein Salzkristall. Dabei vereinen sich die Ionen mit den unterschiedlichen Ladungen (Kation mit Anion usw.). Es bilden sich Elementarzellen (Ez).
In jeder Elementarzelle befinden sich Kationen und Anionen. Stabil ist eine Elementarzelle dann, wenn die Abstände zwischen Kationen und Anionen kurz sind.
Es gibt mehrere typische mathematische Kombinationen. Sie ergeben immer einen typischen Gittertyp. Diese exemplarischen Typen sind nach jeweils einem „prominenten“ Salz benannt.
1. Ein Metallion : ein Anion-Typ (M1X1):
a) CsCl-Typ
1 Anion/ Kation pro Ez
Kz=8
b) NaCl-Typ:
4 Anionen /Kationen pro Ez
Kz=6
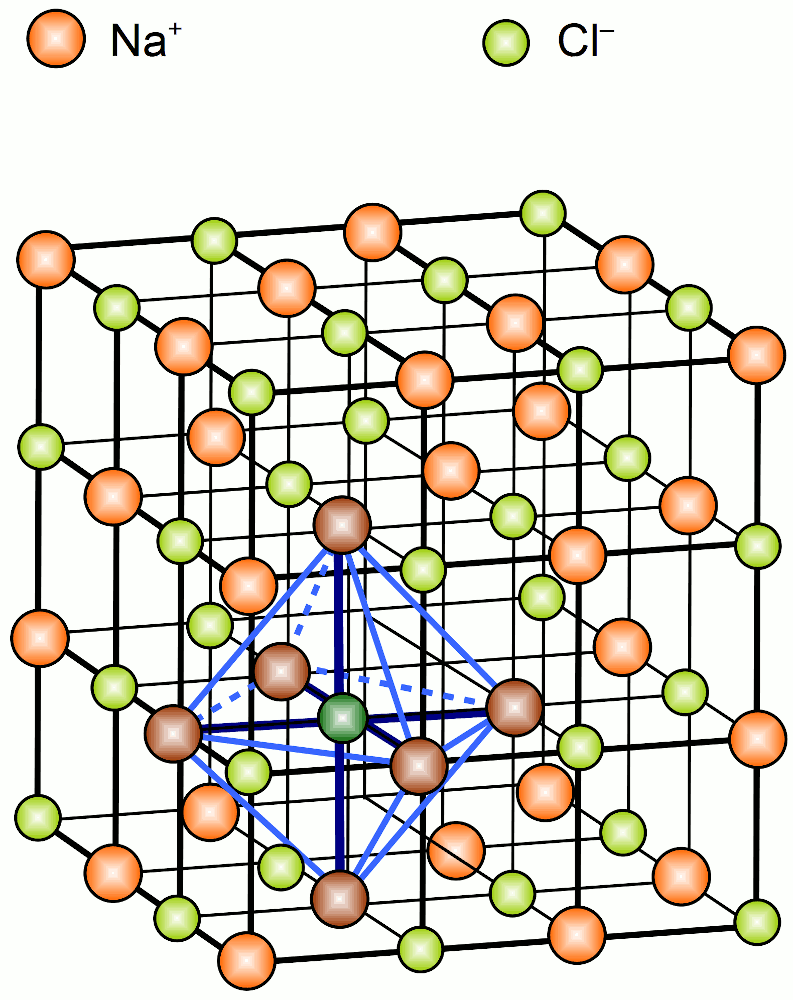
c) ZnS-Typ:
4 Anionen /Kationen pro Ez
Kz=4
d) BN-Typ (ohne größere Bedeutung)
Kz=3
Welcher Typ beim Auskristalisieren entsteht, hängt vom Verhältnis der Radien von Kation und Anion ab:
Übergänge rKation / rAnion:
> 3 : 1 > 2 : 1 > 6 : 1
CsCl-Typ NaCl-Typ ZnS-Typ BN-Typ
2. Ein Metallion : zwei Anionen-Typ (M1X2):
Übergänge und Koordinationszahlen sind entsprechend
a) Fluorit-Typ
b) Rutil-Typ
c) Anitfluorit (oder Cristobalit-)-Typ:
3. Spinell-Typ:
Zwei- und dreiwertige Ionen sind gleichzeitig vorhanden (MgAl2O4). Die dreiwertigen Kationen befinden sich dann in den Tetraederlücken, die zweiwertigen in den Oktaederlücken. Es werden dabei nicht alle Lücken besetzt.
Übersicht über die verschiedenen Kristalltypen
|
Strukturtyp |
Verhältnis der Mindestradien |
Kz Kation |
Kz Anion |
Beispiele |
|
Cäsiumchlorid |
0,732 |
8 |
8 |
CsCl, CsBr, CsI, TlCl, TlI, NH4Cl |
|
Natriumchlorid |
0,414 |
6 |
6 |
LiHal, NaHal, Khal, RbHal (Hal = F, Cl, Br, I) MgS, MgO, CaS, CaO, SrS, SrO, BaS, BaONiS, NiO, AgF |
|
Zinkblende |
0,225 |
4 |
4 |
ZnS, BeS, CdS, CuCl, CuBr, CuI, AgI |
|
Fluorid |
0,732 |
8 |
4 |
CaF2, SrF2,BaF2, CdF2, SrCl2, BaCl2 |
|
Antifluorid |
0,225 |
4 |
8 |
Li2O, Na2O, K2O, Rb2O |
|
Rutil |
0,414 |
6 |
3 |
TiO2, SnO2, MnO2,
MgF2, NiF2, ZnF2 |
Das Coulomb’sche Gesetz
Das Coulombsche Gesetz wurde von dem französischen Physiker Charles Augustin de Coulomb (1736-1806) im Jahre 1785 aufgestellt.
k · (Anz. neg. Ladungen) · (Anz. pos. Ladungen)
EC = —————————————————————————
r
(Anz. neg. Ladungen) · (Anz. pos. Ladungen)
=> EC ~ —————————————————————————
r
EC = Coulomb’sche Energie (hier: Energie, die bei der Gitterbildung frei wird)
r = Abstand der Ladungen zw. den Ionenmittelpunkten (= Kernen)
k= 8,9 · 109 J·m/ C2 (eine Konstante, unveränderbar!)
Allgemein beschreibt das Gesetz die elektrostatische Kraft zwischen zwei Punktladungen. Es besagt, dass diese Kraft proportional zum Produkt dieser beiden Ladungen und umgekehrt proportional zum Quadrat ihres Abstandes ist. Zwei Ladungen mit gleichem Vorzeichen (gleichnamige) stoßen sich ab, solche mit verschiedenem Vorzeichen (ungleichnamige) ziehen sich an.
Das coulombsche Gesetz bildet die Basis der Elektrostatik.
Annahmen:
-
Wenn die Ladungen zweier Ionen das gleiche Vorzeichen haben, ist EC positiv => es ist Energie notwendig, um die Ionen zusammenzubringen.
-
Ist eine Ionenladung aber negativ, ist das Vorzeichen negativ => es wird Energie frei!
-
Ist der Kation - Anion Abstand sehr klein, wird besonders viel Energie frei!
=> Je geringer der Abstand zwischen den Ionen ist, desto mehr Energie muss aufgebracht werden, um das Ionengitter aufzubrechen (Schmelzen).
Wovon hängt die Anziehung also ab?
Die Anziehung hängt von der Anzahl der Ladungen und von den Ionenradien ab.
Berechne, bei welchem Salz die Gitterenergie größer ist: Li+Cl– oder Ag+Cl–
d LiCl = (60pm+181pm) = 241 · 10-12 m
d AgCl = (115pm+181pm) = 296 · 10-12 m
=>
-2/ 241 · 10-12 m = - 0,0083 · 10-12 m
-2/ 296 · 10-12 m = - 0,0068 · 10-12 m => die Energie wird bei AgCl proportional höher sein!
Dies ist die Erklärung für die Tatsache, warum AgCl ein schwerlösliches Salz ist (siehe auch weiter hinten).
Tipps:
- 1 pm sind 0,000 000 000 001m also 10-12 m.
- Ionenradien muss man in Tabellen nachschlagen, niemand weiß sie auswendig, also musst Du sie auch nicht lernen.
Wärme und Kälteeffekte beim Lösen von Salzen
V: Lösen (mit so wenig Wasser wie möglich. z.B.: jeweils 2 ml) verschiedener Salze mit gleichzeitiger Temperaturmessung (vorher Wassertemperatur messen!). Nach Lösen des Salzes wird die Temperatur erneut gemessen.
-
Salze:
T
ΔT
(mögliche Werte)KCl
-7°C
CuSO4
-2°C
CaCl2 · 6H2O
1°C
CaCl2
-7°C
NaCl
0°C
CaO
+2°C
S: Alle Feststoffe die aus Ionen aufgebaut sind, werden als Salz bezeichnet. Im festen Zustand bildet das Salz ein Ionengitter. Wird ein Salz in Wasser gelöst, gehen die Ionen vom unbeweglichen Gitterzustand in den freibeweglichen Zustand über.
Die geschieht in zwei Schritten:
-
Aufbrechen des Ionengitters und freisetzen der Ionen. (Energie wir benötigt, da Ladungen getrennt (auseinander gezogen) werden müssen).
-
An die freien Ionen lagern sich aufgrund elektrostatischer Anziehung Wassermoleküle an (Hydratisierung oder Hydrathüllenbildung). Dabei wird Energie freigesetzt.
Na+ Cl– ---E Gitter---> Na+ + Cl– ---E Hydratisierung ---> Na+(aq) + Cl–(aq)
(wird benötigt) (wird frei)
Das legendäre „Bananenmodell“ der Hydratisierung - Ionen umhüllen sich mit Wasser
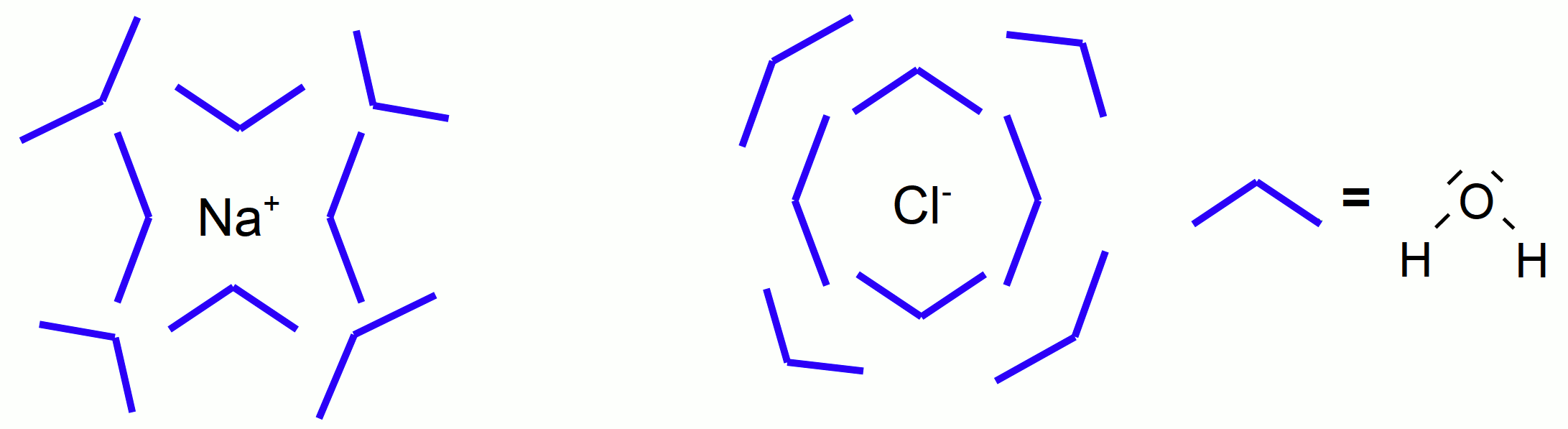
Hhydratisierung von NaCl (Na-Ionen, Cl-Ionen) nach dem "Bananenmodell"
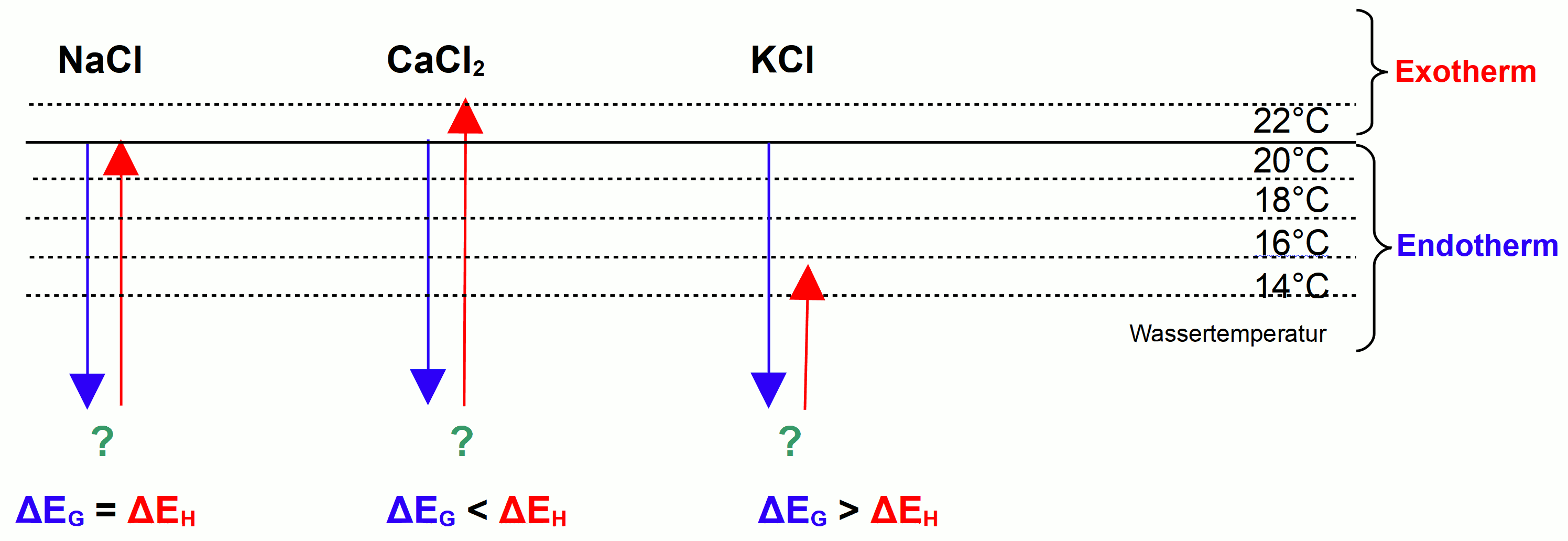
Wärme- und Kälteeffekte beim Lösen verschiedener Salze
Ist der absolute Wert der Hydratationsenergie größer als der der Gitterenergie, kommt es zu einem Temperaturanstieg. Im anderen Fall löst sich das Salz unter Abkühlung.
Bei Salzen bei denen sich die Temperatur verringerte ist die ΔE Gitter > ΔE Hydratisierung
Bei Salzen bei denen sich die Temperatur erhöhte ist die ΔE Gitter < ΔE Hydratisierung
Unterkapitel IV: Fällungsreaktionen und chemische Nachweise
Fällungsreaktionen
Die Energieeffekte, die wir bis jetzt kennengelernt haben, haben natürlich auch praktische Auswirkungen.
Was ist ein schwerlösliches Salz?
Bariumsulfatfällung
Natriumsulfat + Bariumchlorid ---> Bariumsulfat (s) + Natriumchlorid
Salze lösen sich meist gut in Wasser. Treffen aber zwei Ionen zusammen, deren Kombination ein schwer lösliches Salz ergibt, so fällt dieses auch sofort als Feststoff aus (erkennbar am Niederschlag => Trübung). Man nennt dies eine Fällungsreaktion.
Sie ist auch als Nachweis für Ionen geeignet.
In Reaktionsgleichungen wird das Ausfallen eines Stoffes mit einem ↓ oder einem (s) für solid hinter der Summenformel des Stoffs gekennzeichnet.
Durch das Verwenden von spezifischen Fällungsreaktionen ist es möglich, einzelne Bestandteile einer Lösung zu identifizieren, also nachzuweisen. Dies ist sehr wichtig zum Nachweis von Ionen geringer Konzentrationen im Analyselabor. Eine mögliche Anwendung ist die Untersuchung von Trinkwasser oder Lebensmitteln. Fällungsreaktionen können auch zum Ausfällen von störenden Ionen verwendet werden, z.B. bei der Reinigung von Klärwasser in der chemischen Stufe der Kläranlage verwendet werden.
Der Lösungsvorgang bei schwerlöslichen Salzen ist grundsätzlich endotherm. Die zum Lösen benötigte Gitterenergie ist sehr hoch. Die Hydratisierungsenergie reicht hier nicht aus, um das Ionengitter vollständig aufzulösen.
=> Das Salz löst sich nicht auf.
Fällungsreaktionen als chemische Nachweise
V: Kippe die folgenden Lösungen zusammen und untersuche das Ergebnis.
B: In einigen Fällen kommt es zu einer Trübung:
-
KCl
K2SO4
AgNO3
CuSO4
BaCl2
K2CrO4
KNO3
KCl
x
-
AgCl
-
-
-
-
K2SO4
x
-
BaSO4
-
-
AgNO3
x
-
AgCl
Ag2(CrO4)
-
CuSO4
x
BaSO4
Cu(CrO4)
-
BaCl2
x
Ba(CrO4) (gelb)
-
K2CrO4
x
-
KNO3
x
S: Immer wenn ein Feststoff entstanden ist, lag eine Fällungsreaktion vor. Gelöste Ionen haben sich in der Lösung „gefunden“ und ein schwerlösliches Salz gebildet.
Vergleich: Am ehesten kann man Fällungen mit einer Analogie erklären:
Die 10. Klasse fährt im engen Bus ins Schwimmbad. Im Bus sind alle eng zusammen (=Feststoff), im Wasser bewegen sich die Schüler dann wild hin und her. Treffen aber zwei „Verliebte“ aufeinander, so lassen sie sich nicht mehr los und sind (fast) untrennbar verbunden. ;-)
Übersicht über verschiedene Ionennachweise
Ionen sind für den Menschen in der Regel unsichtbar. Um sie nachzuweisen, muss man sie zu einer „sichtbaren“ Form reagieren lassen. Bei vielen Nachweisreaktionen entstehen schwerlösliche oder farbige Verbindungen (Fällungs- oder Farbreaktionen) oder Gase mit auffälligen Eigenschaften.
Zur Kennzeichnung Deiner Reaktionsgleichungen, kannst Du die international gültigen Abkürzungen für die Aggregatzustände verwenden.
(s) = solid
(l) = liquid
(g) = gasförmig
(aq) = in Wasser gelöst
Nachweis von Cl--Ionen
Nachweis durch: Zugabe von Ag+ - Ionen Lösung (z.B. AgNO3)
Beispiel: Cl–(aq) + Ag+(aq) ---> Ag+Cl-(s)↓7
Nachweis => weißer Niederschlag => Fällungsreaktion
Nachweis von Ag+-Ionen
Zum Nachweis von Silberionen verfährt man entsprechend umgekehrt: => Fällungsreaktion
Nachweis von SO42--Ionen
Nachweis durch: Zugabe von Ba2+ Ionenlösung
Beispiel: Ba2+(aq) + (SO4)2–(aq) ---> Ba2+SO42-(s)↓
Nachweis => weißer Niederschlag => Fällungsreaktion
Nachweis von Ba2+-Ionen
Zum Nachweis von Bariumionen verfährt man entsprechend umgekehrt. => Fällungsreaktion
Nachweis von Fe3+-Ionen
Nachweis durch: Zugabe von Cyanatlösung (z.B: Kaliumthiocyanatlösung)
Reaktion: Fe3+(aq) + 3 (SCN)–(aq) ---> Fe3+(SCN-)3
Nachweis => tiefrot
Achtung: Keine Fällungsreaktion, sondern eine Komplexreaktion!
Nachweis von Cu2+-Ionen
Nachweis durch: Zugabe von Ammoniak oder Ammoniakwasser
Reaktion: Cu2+ + 4NH3 ---> [Cu(NH3)4]2+
Nachweis => tiefblaue Farbe (=Kupfertetraminkomplex)
Achtung: Keine Fällungsreaktion, sondern eine Komplexreaktion!
Nachweis von (CO3)2–-Ionen
Nachweis durch: Bei Säurezugabe entsteht Kohlenstoffdioxid, welches als Gas oft am Zischen erkennbar ist.
Reaktion: 2 HCl + (CO3)2– ---> H2CO3 + 2 Cl–
H2CO3 reagiert weiter zu CO2↑ + H2O
Nachweis => Die Lösung schäumt stark auf. (CO2-Bildung)
Keine Fällungsreaktion, da der Nachweis durch die Gasbildung geschieht.
Tabellarische Übersicht über wichtige chemische Nachweisreaktionen
|
Nachzuweisender Soff |
mögl. Nachweissubstanz |
Nachweis durch Bildung von: |
|
|
Ag+ |
NaCl, KCl |
AgCl |
weißer Niederschlag |
|
Ba2+ |
K2SO4 |
BaSO4 |
weißer Niederschlag |
|
Cu2+ |
K2CrO4 |
CuCrO4 |
grüner Niederschlag |
|
Cu2+ |
NH3 |
Cu[NH3]4 |
tiefblaue Farbe |
|
Fe3+ |
KSCN |
FeSCN3 |
tiefrote Farbe |
|
(CO3)2– |
HCl |
CO2 |
aufschäumen |
|
Cl– |
AgNO3 |
AgCl |
weißer Niederschlag |
|
(SO4)2– |
BaCl2 |
BaSO4 |
weißer Niederschlag |
|
(CrO4)2– |
BaCl2 |
BaCrO4 |
gelber Niederschlag |
|
H2 |
O2 (Knallgasprobe) |
H2O |
Knall |
|
O2 |
C (Glimmspanprobe) |
Glimmen |
|
|
CO2 |
Ca(OH)2 (Kalkwasser) |
CaCO3 |
weißer Niederschlag |
Übung: Nachweis von Ionen
Es liegen vier Lösungen in Rundkolben mit BaCl2, KCl und K2SO4 sowie Wasser in einem der Kolben vor.
Leider wurde vergessen, sie zu beschriften. Wie kann man herausfinden, welche Lösung in welchem Kolben ist?
Es wird nur ein Teil der Ionen nachgewiesen d.h. ein Schluss von Cl– auf z.B. NaCl ist nur unter diesen Voraussetzungen möglich.
|
z.B. |
Lösung 1 |
Lösung 2 |
Lösung 3 |
Lösung 4 |
|
AgNO3 |
||||
|
CuSO4 |
||||
|
K2SO4 |
||||
|
BaCl2 |
Aufstellen der Fällungsgleichungen für alle Niederschläge => Welche Salze sind schwerlöslich?
NS mit AgNO3:
NS mit BaCl2:
Wozu dienen Fällungsreaktionen? Wasseruntersuchungen
Ein Labor hat 4 Wasserproben (3 Mineralwasser und ein destilliertes Wasser) auf ihren Ionengehalt untersucht und leider zur Befestigung der Etiketten einen schlechten Klebstoff verwendet. Die Schilder sind abgefallen. Ist jetzt noch möglich, die einzelnen Wasserproben den Laborergebnissen zuzuordnen?
Inhaltstoffe
-
Wie unterscheiden sich die Wasser?
-
Wisst ihr etwas über für den Körper brauchbare/ schädliche Ionen?
-
Welche Ionen habt ihr den schon nachgewiesen?
Versuch: Analyse dreier Mineralwasser
Drei Flaschen Mineralwasser und destilliertes Wasser werden in gleichen Bechergläsern präsentiert.
Die Schüler sollen eine Zuordnung zu den Originalquellen versuchen.
Versuch: Nachweis von Chlorid und Sulfationen in:
a) Mineralwasser 1
b) Mineralwasser 2
c) Mineralwasser 3
d) Destilliertes Wasser
B: Unterschiedliche Trübungen, je nach Ionengehalt. => Zuordnung möglich!
Schlussfolgerung & Auswertung:
-
Welche zwei schwerlöslichen Salze haben wir gebildet?
-
Kann man mit unseren Erfahrungen jetzt den Chloridgehalt von Leitungswasser bestimmen?
-
Warum kann die ursprünglich „mindergiftige“ Bariumionenlösung unbeschadet in den Ausguss?
Ja, denn Bariumsulfat ist ein als Mineral (Barit) sehr schlecht löslich! Es löst sich noch nicht mal in HCl! -
Einige Wasser tragen die Aufschrift: „Enteisent“. Wie ist es möglich ein Ion gezielt zu entfernen.
-
Warum entfernt man nicht auf demselben Wege Chloridionen aus dem Wasser?
-
Beim Erhitzen von Wasser werden (durch komplizierte Reaktionen) Carbonate freigesetzt. Diese reagieren mit Calciumionen zu einem schwerlöslichen Salz. Wie heißt es und was für Folgen hat dies?
Laborergebnisse
Ordne die Wasserproben den entsprechenden Marken zu:
|
Wasser 1 [mg/l] |
Wasser 2 [mg/l] |
Wasser 3 [mg/l] |
|
|
Probe Nr.:
|
Probe Nr.: |
Probe Nr.: |
|
|
Na+ |
3,6 |
27,5 |
228 |
|
K+ |
11,5 |
12,5 |
26,7 |
|
Mg2+ |
26,5 |
51,5 |
36,1 |
|
Ca2+ |
55,5 |
380,0 |
186 |
|
Cl- |
10,1 |
30,9 |
121 |
|
SO42- |
60,0 |
549,0 |
42 |
|
NO3- |
<0,5 |
<0,1 |
<0,1 |
Kategorien von Trinkwassern
Natürliches Mineralwasser:
Es hat seinen Ursprung in einem unterirdischen, vor Verunreinigungen geschützten Wasservorkommen und wird aus einer oder mehreren natürlichen oder künstlich erschlossenen Quellen gewonnen. Es ist durch seinen Ursprung von hoher Reinheit („ursprüngliche Reinheit“) und es sind für dieses Wasser keine Grenzwerte definiert.
Es enthält für Menschen wichtige Mineralstoffe, Spurenelemente und evtl. andere Bestandteile.
Quellwasser:
Quellwasser stammt aus unterirdischen Wasservorkommen. Der Unterschied zu natürlichem Quellwasser liegt darin, dass es nicht von ursprünglicher Reinheit sein muss. Das heißt, es dürfen sich innerhalb der Grenzwerte auch Schadstoffe darin befinden.
Tafelwasser:
Es wird auch „künstliches Mineralwasser“ genannt und kann aus Trinkwasser oder aus einer Mischung von Trink- und natürlichem Mineralwasser gewonnen werden.
Heilwasser:
Es unterliegt dem Arzneimittelgesetz! Teilweise hat es einen sehr hohen Gehalt an einzelnen Mineralsalzen. Mit einem Liter pro Tag kann der Tagesbedarf des Menschen schon überschritten werden.
Unterkapitel V: Zusammenfassung, Tipps und wichtige Hilfen
Unterscheidung der Stoffe chemischer Reaktionen
1. In der Chemie verwendet man meist drei Typen von Stoffen:
a) Elemente: (stehen im PSE)
Ihre Formel ist immer so, wie sie dort stehen (z.B. Mg oder Fe), bis auf die Ausnahmen Wasserstoff (H2), Stickstoff (N2), Sauerstoff (O2) und die Elemente der 7. Hauptgruppe (F2, Cl2, Br2, I2).
Diese liegen immer als 2fach Molekülelement vor. Elemente haben keine Ionenladung!
b) Ungeladene Molekülverbindungen aus mehren Elementen: (z.B. H2O, CO2 oder NH3)
Es handelt sich hierbei in der Regel um Nichtmetallverbindungen. Ihre Formel muss man kennen (also lernen).
Achtung! Es gibt aber auch Moleküle mit Ionenladungen. Dazu gehören zum Beispiel die Säurereste. Diese Ladungen musst Du lernen - da hilft alles nichts!
c) Salze und Oxide:
Hier liegen Ionen vor. Die Ladungen kannst Du oft im Periodensystem an der Hauptgruppennummer ablesen! (Erklärung siehe unten)
(Typische Salze: KCl, Na2SO4, Ca3(PO4)2; typische Oxide: CuO, Fe2O3, Na2O)
3 Möglichkeiten Ionenreaktionen zu notieren
1. Vollständige Salze angeben (mit oder ohne Ionenladung):
Salze: Ba(NO3)2 (aq) + Mg(SO4) (aq) ---> Mg(NO3)2 (aq) + Ba(SO4) (s)
Salze mit Ionenladungen: Ba2+(NO3)–2 (aq) + Mg2+(SO4)2– (aq) ---> Mg2+(NO3)–2 (aq) + Ba2+(SO4)2– (s)
Beachte:
-
Gelöste Salze werden mit (aq) abgegeben. Das bedeutet, dass die Ionen gelöst in Wasser, also hydratisiert sind. Feststoffe werden mit (s) „solid“ gekennzeichnet ((l) für Flüssigkeiten, (g) für Gase).
-
Bariumsulfat ein Feststoff, also nicht gelöst!
2. Salze in einzelne Ionen aufführen: (immer mit Ionenladung!):
Diese Methode kann man verwenden, wenn die Ionen freibeweglich, also in Wasser aufgelöst sind:
Ba2+(aq) + 2 (NO3)–(aq) + Mg2+(aq) + (SO4)2–(aq) ---> Mg2+(aq) + 2 (NO3)–(aq) + Ba(SO4) (s)
Beachte: Auch hier ist Bariumsulfat ein Feststoff, also nicht gelöst und muss deshalb als komplettes Salz notiert werden!
3. Weglassen der Ionen, die an der eigentlichen Reaktion nicht teilnehmen:
Ba2+ (aq) + (SO4)2– (aq) ---> Ba2+(SO4)2– (s)
Um Reaktionsgleichungen übersichtlicher zu gestalten, kann man Ionen, die bei der Reaktion nicht teilnehmen weglassen. Man sollte aber immer daran denken, dass sie trotzdem vorhanden sind!
Wiederholungsfragen Ionen
Ionen & Salze
-
Nenne typische Eigenschaften von Salzen.
-
Was ist ein Ion? Definiere,
-
Erkläre den Begriff Edelgaskonfiguration.
-
Nenne verschiedene Möglichkeiten Natriumchlorid zu bilden. Schlage jeweils einen geeigneten Aufbau vor.
-
Nenne die Regeln, nach denen man die Ionenladung eines Ions bestimmen kann.
-
Beschreibe den Versuch zur Ionenwanderung. Welche Beobachtung kann man bei Kupfersalzen, bei Kaliumpermanganat und bei Kaliumdichromat machen. Erkläre diese Beobachtungen.
-
Bestimme die Ionenladung der folgenden Ionen und erstelle die Summenformel, welche sie im entsprechenden Salzkristall haben:
|
Cl |
Br |
O |
SO3 |
|
|
Li |
||||
|
Ba |
||||
|
Mg |
||||
|
Al |
-
Stelle die folgenden Reaktionsgleichungen auf und kennzeichne dabei alle Ionen:
a) Ammoniumcarbonat reagiert zu Ammoniak, Kohlendioxid und Wasser.b) Ammoniumhydrogensulfit zerfällt in Ammoniak, Schwefeldioxid und Wasser
c) Reaktion von Natriumhydrogencarbonat mit Schwefelsäure. Es entstehen Kohlendioxid, Natriumsulfat
und ein dritter, Dir bekannter Stoff.d) Kaliumhydrogencarbonat wird durch Hitze zu Kohlendioxid, Wasser und einem dritten Stoff zersetzt.
e) Reaktion von FeS2 mit Sauerstoff zu Eisen(III)-oxid und Schwefeldioxid.
-
Beschreibe den Versuchsaufbau der Elektrolyse von Kupferchlorid. Welche Beobachtungen kann man machen? Erkläre diese.
-
Betrachte die Bildung von Natriumchlorid unter energetischem Aspekt im Detail. Welche Einzelschritte laufen ab?
-
Sind diese endo- oder exotherm? Versuche dies jeweils anhand einer Modellvorstellung zu erklären.
-
Warum ist die Reaktion insgesamt exotherm?
-
Definiere die Begriffe Ionisierungsenergie und Elektroaffinitätsenergie.
-
Warum hat Natriumchlorid die Summenformel NaCl?
-
Was versteht man unter dem Begriff „Koordinationszahl“?
-
Wovon hängt die Koordinationszahl ab?
-
Nenne und erkläre die Coulomb’sche Formel.
-
Erkläre den Vorgang des Schmelzens. Wovon ist der Schmelzpunkt abhängig?
-
Warum leiten Ionen den elektrischen Strom? Beschreibe einen entsprechenden Versuch.
-
Welche Ionen sind in Natriumchlorid zu finden? Welche in Berylliumsulfat?
-
Ionen entstehen durch...
-
Ionen unterscheiden sich von Atomen durch...
-
Beschreibe den Aufbau der Salze. Nenne Möglichkeiten sie chemisch zu bilden.
-
Welche Eigenschaften haben Ionen?
-
Wie bestimmt man die Ladung eines Säurerestes? Welche Ladung hat der Säurerest der Chromsäure H2Cr2O7 und der der Kieselsäure H2SiO3?
-
Welche Voraussetzungen müssen gegeben sein, damit Ionen den Strom leiten?
-
Stelle die folgenden Reaktionsgleichungen auf: (Tipp: Bilde Ionen aus der Schwefelsäure)
a) Schwefelsäure + Wasser
b) Schwefelsäure + Magnesium -
Erkläre den Begriff Ionenbindung. Wodurch werden die Ionen im festen Aggregatzustand zusammengehalten?
-
Wozu dienen Fällungsreaktionen? Nenne Beispiele.
-
Erkläre das allgemeine Prinzip eines Nachweises. Nenne mindestens 6 chemische Nachweise.
- Warum hat Natriumchlorid die Summenformel NaCl? Wäre Na1000Cl1000 nicht passender?
-
Erkläre den Vorgang des Schmelzens eines Salzes. Wovon ist der Schmelzpunkt abhängig?
Fußnoten:
=> das Salz löst sich nicht (nur in sehr geringen Mengen), solange nicht mehr Energie zugeführt wird.
3Auch wenn Menschen die Röntgenstrahlen nicht sehen können, so ist die Photoplatte dafür doch sensibel. Röntgenstrahlen schwärzen die Stellen, auf die sie treffen (denn es ist ja ein Negativ!). Nach der Entwicklung sind diese Stellen dann hell (siehe auch Abbildung)
4Damit das Ionengitter richtig fest und stabil ist, muss der optimale Abstand zwischen den Ionen vorliegen. Ist er zu groß, wäre das Gitter zu locker (zu geringe Anziehungskraft), ist er zu gering, würden sich die Atomkerne zu stark abstoßen.
5Siehe auch „Die Teilschritte der NaCl-Bildung“.
6Die Edelgasregel ist allerdings ein geeignetes Hilfsmittel bei der Aufstellung der Ionen, die an der Salzbildung beteiligt sind.
7Der Pfeil ↓ bedeutet, dass dieser Feststoff ausfällt, d.h. sich am Boden abscheidet.
