Kapitel 16: Säure - Base - Reaktionen (nach dem Donator-Akzeptor-Prinzip)

Säuren und Laugen begleiten uns täglich – ohne sie wäre ein zivilisiertes Leben nicht möglich!
Säure-Base-Chemie - Wdh. 9. Klasse
Erinnerst Du Dich an die Eigenschaften und Besonderheiten von Säuren und Laugen? Hier noch mal eine kurze Wiederholung, wenn Du Dich nicht mehr erinnerst, dann lese doch noch mal das Kapitel 4.
-
Säure und Laugen ätzen.
-
Sie werden durch Indikatoren für uns erkenntlich gemacht. Oft verwendet man Universalindikator. Er zeigt bei Säuren die Farbe rot, bei neutralen Lösungen grün und bei Laugen blau.
-
Säuren greifen v.a. unedle Metalle an, Laugen greifen v.a. organische Substanzen an.
-
Natronlauge und Kalilauge liegen als Feststoff vor und müssen vor dem Gebrauch erst aufgelöst werden.
-
Säures und Laugen sind „Gegenspieler“, die sich bei gleicher Konzentration in ihrer Wirkung aufheben. Diesen Vorgang nennt man Neutralisation. Diesen Vorgang nennt man Neutralisation:
H+ + (OH)– ---> H2O -
Säuren enthalten in ihrer Formel alle Wasserstoffionen (=Protonen), Laugen sind wässrigen Hydroxidlösungen (enthalten (OH)–).
-
Chlorwasserstoffsäure nennt man in Wasser gelöst auch Salzsäure.
-
Laugen sind wässrige Hydroxidlösungen.
-
Natriumlauge = Natronlauge = Natriumhydroxid.
-
Kaliumlauge = Kalilauge = Kaliumhydroxid
Die wichtigsten Säuren und ihre Säurereste |
|
Säure: |
Säurerest: |
||
|
HF |
Fluorwasserstoffsäure |
F– |
Fluorid |
|
HCl |
Chlorwasserstoffsäure |
Cl– |
Chlorid |
|
HBr |
Bromwasserstoffsäure |
Br– |
Bromid |
|
HI |
Iodwasserstoffsäure |
I– |
Iodid |
|
H2S |
Schwefelwasserstoff(säure) |
S2– |
Sulfid |
|
H2O |
Wasser (Sonderfall!) |
O2– |
Oxid |
|
HCN |
Blausäure |
CN– |
Cyanid |
|
HNO3 |
Salpetersäure |
(NO3)– |
Nitrat |
|
H2SO4 |
Schwefelsäure |
(SO4)2– |
Sulfat |
|
H2CO3 |
Kohlensäure |
(CO3)2– |
Carbonat |
|
H3PO4 |
Phosphorsäure |
(PO4)3– |
Phosphat |
|
HNO2 |
Salpetrigesäure |
(NO2)– |
Nitrit |
|
H2SO3 |
Schwefeligesäure |
(SO3)2– |
Sulfit |
|
Die wichtigsten Laugen |
|
Lauge: |
|
|
NaOH |
Natronlauge |
|
KOH |
Kalilauge |
|
Ca(OH)2 |
Calciumlauge (=Kalkwasser) |
|
Ba(OH)2 |
Bariumlauge (=Barytwasser) |
|
Mg(OH)2 |
Magnesiumhydroxid |
Als erster definierte der Chemiker Svante Arrhenius (1887), was Laugen und Säuren sind: Laugen sind wässrige Hydroxidlösungen.
Säuren sind Stoffe, die beim Auflösen in Wasser Protonen (H+) abgeben.
Weitere anorganische und organische Säuren
Es gibt noch viele andere Säuren. Wenn sie auf Kohlenstoffen beruhen, nennen wir diese organische Säuren. Diese Säuren kennst Du vielleicht aus der Biologie oder von Lebensmitteln. Dazu gehören Essigsäure, Ameisensäure, Ascorbinsäure und viele mehr. Diese Säuren wirst Du in der Oberstufe besser kennenlernen (siehe auch OC-Kapitel „Carbonsäuren“).
a) Weitere anorganische Säuren
Kieselsäure: H2SiO3
Arsensäure: H3AsO4
Eine große Gruppe stellen die Halogensauerstoffsäuren dar:
Sie sind vom Aufbau her: H(Halogen)O, H(Halogen)O2, H(Halogen)O3, H(Halogen)O4
Die bekanntesten sind dabei die Chlorsauerstoffsäuren:
-
Hypochlorige Säure: HClO
-
Chlorige Säure: HClO2
-
Chlorsäure: HClO3
-
Perchlorsäure: HClO4
Von Fluor gibt es vermutlich nur die Hypofluorige Säure (HOF).
Von Brom gibt es:
Hypobromige Säure : HBrO
Bromige Säure: HBrO2
Bromsäure: HBrO3
Perbromsäure: HBrO4
Von Iod gibt es eine enorme Anzahl an Sauerstoffsäuren:
Hypoiodige Säure: HIO
Iodige Säure: HIO2
Iodsäure: HIO3
Metaperiodsäure: HIO4
Mesoperiodsäure: H3IO5
Orthoperiodsäure: H5IO6
Metadiperiodsäure: H4I2O9
Mesodiperiodsäure: H6I2O10
Orthodiperiodsäure: H8I2O11
Wie man sieht, ist die Natur da sehr erfindungsreich. Keine Sorge, diese Säuren müsst ihr nicht lernen!
b) Dissoziation der anorganischen Säuren
Unter der Dissoziation versteht man generell den Zerfall oder die Zersetzung eines Verbindung. Diese läuft normalerweise immer mit einem Partner ab. Die folgenden Reaktionsgleichungen sollen zeigen, was mit einer Säure dabei passiert. Der Reaktionspartner wurde also bewusst mal weggelassen!
Man sieht, dass eine Säure immer mindestens ein Wasserstoffion (H+) abgibt. Dieses Teilchen nennen wir auch Proton, da Wasserstoff ja kein Neutron hat und als Ion sein Elektron abgegeben hat.
Bei dieser theoretischen Reaktion (ohne Partner) bleibt der Säurerest über:
Kieselsäure: H2SiO3 ---> H+ + (HSiO3)– ---> 2H+ + (SiO3)2–
Hydrogensilikat Silikat
Arsensäure: H3AsO4 ---> 3H+ + (AsO4)3–
Arsenat
Hypochlorige Säure (=Chlor(I)-säure): HClO ---> H+ + (ClO)–
Hypochlorit
Chlorige Säure (=Chlor(III)-säure): HClO2 ---> H+ + (ClO2)–
Chlorit
Chlorsäure (=Chlor(V)-säure): HClO3 ---> H+ + (ClO3)–
Chlorat
Perchlorsäure (=Chlor(VII)-säure): HClO4 ---> H+ + (ClO4)–
Perchlorat
c) Organische Säuren
Organische Säuren kommen in der Natur als Produkt von Tieren oder Pflanzen vor. Sie unterscheiden sich in ihrem Aufbau, da sie nur aus Kohlenstoff-, Wasserstoff- und Sauerstoffatomen bestehen (bei Aminosäuren ist auch Stickstoff enthalten). Ihre Wirkung ist meist etwas schwächer. Einige werden sogar als Lebensmittel eingesetzt. Es gibt Tausende! Ihre Formeln sind oft komplizierter:
Essigsäure: C2H4O2
Säurerest: Acetat Abkürzung Essigsäure: HAc
Zitronensäure: C6O7H8
Säurerest: Citrat
Ameisensäure: CH2O2
Säurerest: Formiat
Oxalsäure: C2H2O4
Säurerest: Oxalat
Äpfelsäure: C4H6O5
Säurerest: Malat
Ascorbinsäure (=Vit C): C6H8O6
Säurerest: Ascorbat
Bernsteinsäure: C4H6O4
Säurerest: Succinat
Acetylsalicylsäure (=Aspirin) C9H8O4
Säurerest: Acetyl-Salicylat
Bei Essigsäure kann man einen Trick verwenden: Man tut so, als sei sie anorganisch und somit besteht sie aus H+ und dem Säurerest Ac- (Acetat). Ac also nicht mit dem Element Actinium verwechseln!
Zusatzinformationen:
https://de.wikipedia.org/wiki/Halogensauerstoffsäuren
Formeln von einigen ausgewählten organischen Säuren
Monocarbonsäuren: Ameisensäure, Essigsäure
Dicarbonsäuren: Oxalsäure, Bernsteinsäure
Hydroxycarbonsäuren: Äpfelsäure, Zitronensäure
Säuren mit aromatischen Ring: Acetylsalicylsäure, Ascorbinsäure
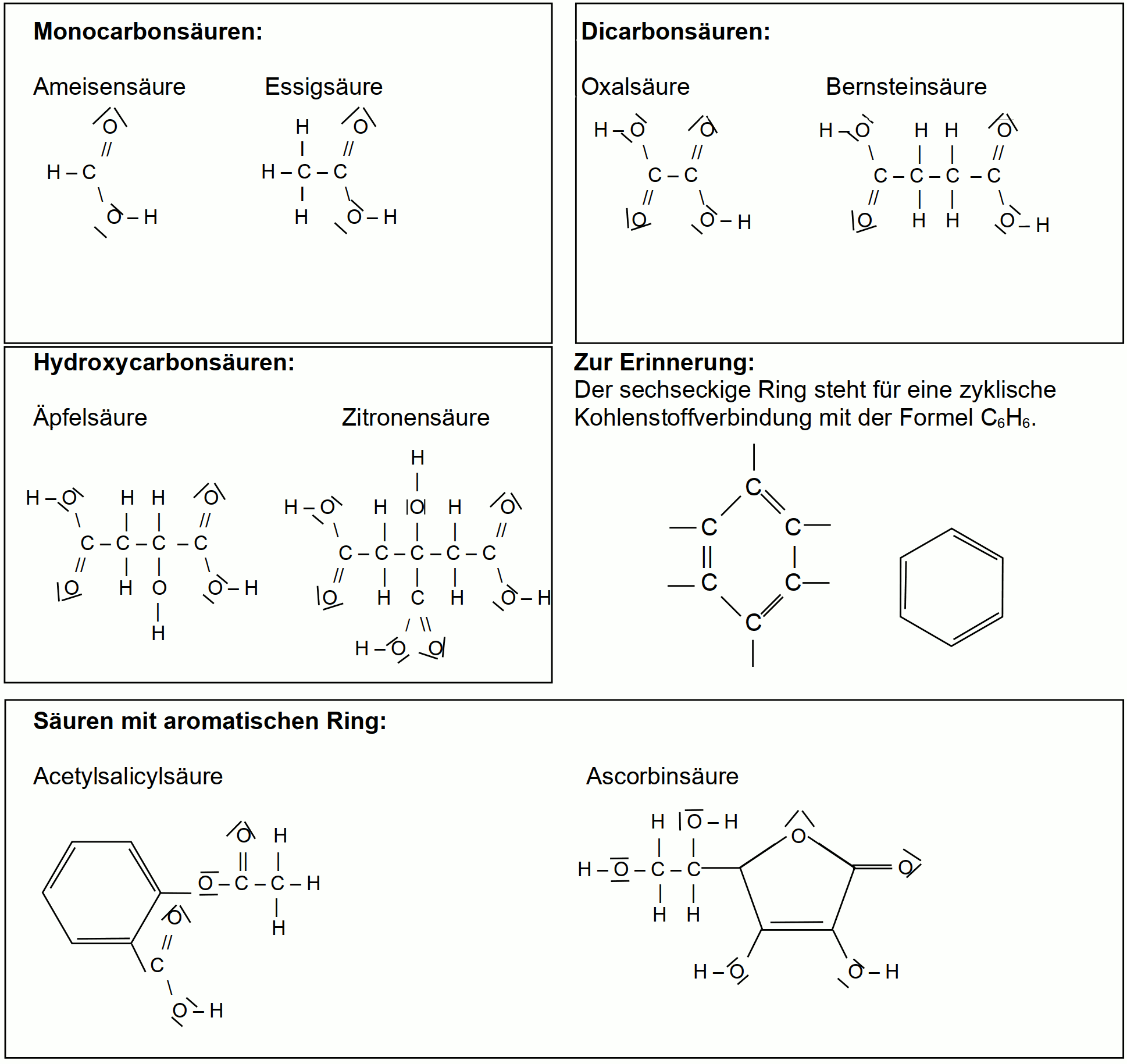
Darstellung von Chlorwasserstoff (HCl)
Material: Gasentwicklungsapparatur, Thermometer, Leitfähigkeitsmessung
V1: Konzentrierte Schwefelsäure (H2SO4) wird aus einem Tropftrichter auf feuchtes NaCl getropft (Reaktion1).
V2: Das entstehende Produkt wird über einen Schlauch über Wasser (in einer eine Glaswanne) geleitet. Die Stromstärke und der Säuregrad werden gemessen (Reaktion2).
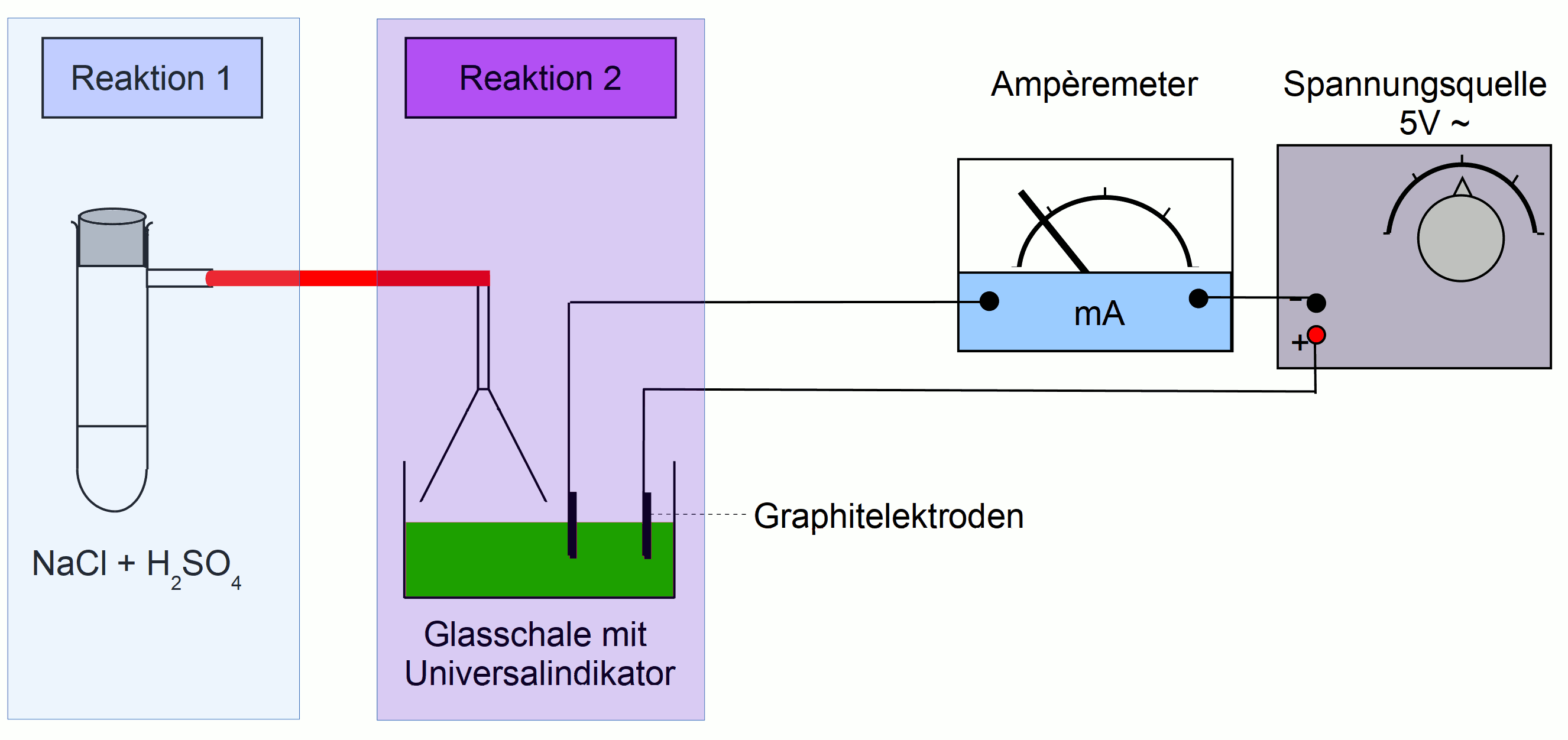
Skizze der Gasentwicklungsapperatur zur Darstellung von Chlorwasserstoff (HCl)
|
B1 |
S1 |
|
Schaumbildung,
|
HCl ist ein Gas! Bei der Bildung wird Energie frei (exotherme Reaktion). Merke: Säuren können in allen Aggregatzuständen vorkommen! |
|
Wärmeentwicklung, das Gefäß wird heiß |
Bei der Bildung von HCl wird viel Energie frei. |
=> H2SO4 + 2 NaCl ---> 2 HCl + Na2SO4 + E
Zur Entstehung von Chlorwasserstoff muss man wissen, dass dieser eine minimal schwächere Säure als Schwefelsäure ist. Es gilt die Regel: Die stärkere Säure (hier Schwefelsäure) treibt die schwächere Säure (hier Chlorwasserstoff) aus ihrem Salz (hier Natriumchlorid).
|
B2 |
S2 |
|
Das Gas löst sich im Wasser |
HCl löst sich ausgesprochen gut in Wasser1. Es findet eine Reaktion statt. |
|
Universalindikator färbt sich rot |
=> es hat sich eine Säure gebildet. |
|
Die Temperatur steigt |
=> es liegt eine exotherme Reaktion vor. |
|
Die Leitfähigkeit steigt |
=> es bilden sich Ionen - Ursache muss eine heterolytische (=ungleiche) Spaltung des HCl in Ionen sein. |
Wichtig: Wie kann man feststellen, welche Ionen in der Glasschale enthalten sind?
Man gibt Silbernitratlösung zu. Die Zugabe von AgNO3 zeigt eine weiße Trübung. Es liegt also eine Fällungsreaktion vor! Siberionen sind ein Nachweis für Chloridionen!
=> Es sind Chloridionen enthalten, es bildet sich das schwerlösliche Salz Silberchlorid.
=> HCl + H2O ---> Cl– + ?
Welcher weiterer Stoff kann entstanden sein? Das ist nun nicht ganz trivial.
Die Lösung liefert der folgende Abschnitt.
Die Protolyse
Die Auflösung der Frage, welcher Stoff bei der Reaktion von HCl mit H2O entstanden ist, ist nicht so einfach, da ein neues, Dir bis jetzt unbekanntes Teilchen entstanden ist.
Was wissen wir bereits?
Cl– entsteht => HCl musste dazu gespalten wurden sein:
![]()
Kurzzeitig entsteht also ein Proton und Chlorid.
Aber wie kommt es zu dieser ungleichen (=heterolytischen) Spaltung des HCl?
Erinnere dich: HCl und H2O sind Dipol-Moleküle! Das Wasserstoffatom des HCl ist partial positiv geladen und wird also auch leicht vom Sauerstoffatom des Wassers angezogen, da dieses eine negativ Partialladung hat. Da Sauerstoff insgesamt elektronegativer als Chlor ist, verliert Chlor diesen „Kampf“ um sein Wasserstoffatom (vergleiche mit den Elektronegativitätswerten unter dem Bild!).
Die Folge ist, dass Wasserstoff (allerdings ohne die Bindungselektronen, den an denen zieht Chlor zu stark!) den Bindungspartner wechselt:

Elektronegativitäten: Cl: 3,0; H: 2,1; O: 3,5
Merke: Der Sauerstoff des Wassers ist partial negativ geladen.
Er übt so eine Anziehungskraft auf das Wasserstoffatom des Chlorwasserstoffes aus.
Wasserstoff verlässt seinen ursprünglichen Partner.
Dabei lässt Wasserstoff seine Bindung zurück, da er sonst zweibindig wird, was aber nicht möglich ist.
Die Konsequenz ist, dass HCl heterolytisch getrennt wird. Dabei wird dem elektronegativeren Atom das Elektronenpaar „zugeteilt“.
Es entstehen H+ und Cl–.
Das Video zum Versuch findet ihr in meinem Kanal: https://www.youtube.com/watch?v=0R-PFjdf1IQ
Was passiert als nächstes? Das freie Elektronenpaar des Sauerstoffs „klappt“ nun auf und geht so eine Bindung mit dem Wasserstoff ein und bildet so ein Oxoniumion (H3O+).
Oxonium wurde früher auch „Hydroniumion“ genannt. Der Ausdruck „Hydroxonium“ ist ebenso veraltet!
Man könnte vereinfacht sagen, das Sauerstoffatom des Wassers „flirtet“ mit dem Wasserstoff (des HCl), indem er es in „Versuchung“ bringt, sodass Wasserstoff letztlich untreu wird und seinen Partner „verlässt“.
Bei der „Trennung“ von Wasserstoff und Chlor bleibt das gemeinsame Eigentum (also die Elektronen) bei dem Verlassenen.
Sauerstoff hingegen hat nun einen dritten Wasserstoff, was er als zweitelektronegativstes Element auch kann. Alles in allem eine melodramatische Geschichte. ;-)
Diese Reaktion ist exemplarisch für so viele Reaktionen, die nach dem gleichen Prinzip ablaufen, sodass man dieser Reaktionsart einen eigenen Namen gegeben hat:
Die Säure-Base-Reaktion
Wenn man sich die letzte Reaktionsgleichung ansieht, dann kann man sehen, dass ein Proton den Reaktionspartner gewechselt hat. Diese Art der Reaktion nennen wir Protolyse oder Säure-Base-Reaktion.
Um das zu verstehen, müssen wir einige neue Definitionen einführen.
Der erste Chemiker, der sich mit der Thematik beschäftigte, war der schon erwähnte Svante Arrhenius. Seine Definition des Begriffes Lauge war zwar richtig, aber sie deckte nicht alle alkalischen Reaktionen ab. Es gab Stoffe, wie NH3, die zwar in Wasser alkalisch reagieren, aber kein Hydroxid enthalten (siehe auch ein paar Seiten weiter: „Ist Ammoniak (NH3) eine Lauge?“).
Diesen Widerspruch konnten Brönsted und Lowry auflösen, indem sie auf das Hydroxid verzichteten und sich einfach auf die Wasserstoffionen bezogen:
Säuren sind Stoffe, die Protonen (H+) abgeben können (= Protonendonatoren).
Basen sind Stoff, die Protonen (H+) aufnehmen können (= Protonenakzeptoren).
Erinnere Dich: Da H+ keine Elektronen hat und nur ein Proton (und kein Neutron!), wird es unter Chemiker auch als Proton bezeichnet!
Bei Säure-Base-Reaktionen (Protolyse) wird ein H+ von einem Partner auf einen anderen übertragen.
Beispiele:

Beachte: Ein Stoff (wie z.B. HCl) ist also erst in Verbindung mit Wasser eine Säure. Säure ist demnach nicht eine Stoffeigenschaft, sondern erst das Ergebnis einer Reaktion, bei der Oxoniumionen entstehen.
Man spricht auch von der sauren Reaktion. Bei einer Base ist dies genauso, sie ist für die alkalische Reaktion verantwortlich.
Aufgaben zur Protolyse:
- Erstelle Gleichungen für die Protolyse von 8 Säuren.
- Erstelle die Reaktionsgleichung der Reaktion von HF in Wasser. Wie nennt man so einen Protonenübergang?
- Definieren die Begriffe Base und Säure nach Brönstedt.
- NaHCO3 reagiert mit Wasser und zugegebener Universalindikator zeigt eine blaue Farbe an (alkalisch). Formuliere die Protolysegleichung.
- NaHSO4 reagiert mit Wasser und zugegebener Universalindikator zeigt eine rote Farbe an (sauer). Formuliere die Protolysegleichung.
- Beschrifte das Foto und benenne alle Bauteile. Mache Dir Gedanken über das Glasrohr, welches mit dem rosa Pfeil gekennzeichnet ist. Wozu ist es notwendig?

Versuchsaufbau der Darstellung von HCl
Zusatzinformationen:
- https://de.wikipedia.org/wiki/Protolyse
- https://de.wikipedia.org/wiki/Salzsäure
- https://de.wikipedia.org/wiki/Chlorwasserstoff
Das korrespondierende Säure-Base-Paar
Wenn man nun bei einer Säure-Base-Reaktion Säure und Base zugeordnet hat, so könnte man sich doch auch die Reaktion „zurück“ vorstellen. Diese Reaktion nennen wir „Rückreaktion“. Auch diese kann stattfinden. Dies geschieht vor allem bei schwächeren Säuren:

Wenn also die Rückreaktion auch stattfinden kann, und selbst wenn es nur in unserer Vorstellung ist, dann kann man also auch den Produkten die Begriffe Säure und Base zuordnen.
Dabei kann man nun Pärchen finden:
H2S ---> S2–
Säure Base
2H2O ---> 2H3O+
Base Säure
Wie man sieht reagiert eine Säure zu ihrer passenden (korrespondierenden) Base und umgekehrt. Das ist ja auch logisch: Wenn eine Säure sauer reagiert, weil sie ihr Proton abgibt, dann kann der aus der Säure entstandene Rest ja auch irgendwann wieder ein Proton aufnehmen (und umgekehrt).
Eine Säure reagiert durch Abgabe von Protonen zu ihrer korrespondierenden Base.
Eine Base reagiert durch Protonenaufnahme zu ihrer korrespondierenden Säure.
=> An einer Säure-Base-Reaktion sind stets zwei korrespondierende Säure-Base-Paare beteiligt.
Die Eigenschaften saurer wässriger Lösungen sind auf Oxoniumionen (H3O+), die Eigenschaften alkalischer wässriger Lösungen auf Hydroxidionen (OH–) zurückzuführen.
(Übrigens: den neuen Reaktionspfeil brauchst Du in der Mittelstufe noch nicht verwenden!)
Aufgaben:
1. Kennzeichne in den beiden folgenden Säure-Base Reaktionen jeweils Säuren und Basen und dann die korrespondierenden Säure-Base Paare:
H2SO4 + Cl– ---> (HSO4)– + HCl
HCl + H2O ---> H3O+ + Cl–
HCN + KOH ---> K+ + H2O + CN–
HNO3 + OH– ---> H2O + (NO3)–
H3O+ + OH– ---> 2H2O
Zusatzinformationen:
- https://de.wikipedia.org/wiki/Protolyse
- https://de.wikipedia.org/wiki/Salzsäure
- https://de.wikipedia.org/wiki/Chlorwasserstoff
Zusammenfassung: Definitionen und Konzept der Säure-Base Chemie
Säure und Lauge-Begriff Arrhenius:
Eine Säure ist ein Stoff, der in wässriger Lösung Wasserstoffionen freisetzt.
Eine Lauge ist ein Stoff, der in wässriger Lösung Hydroxidionen freisetzt.
Säure und Base-Begriff nach Brönsted und Lowry:
Säuren sind Stoffe, die Protonen abgeben können (Protonendonatoren).
Basen sind Stoff, die Protonen aufnehmen können (Protonenakzeptoren).
Beachte den Unterschied:
Lauge: Stoff der Hydroxidionen bildet.
Base: Stoff der Protonen aufnehmen kann.
Bei Säure-Base-Reaktionen werden Protonen von der Säure auf die Base übertragen.
Korrespondierende Säure-Base-Pärchen
Protolysegleichung von HBr
HBr + H2O ---> Br – + H3O+
Säure Base Base Säure
Eine Säure braucht immer eine Base, mit der sie reagieren kann und umgekehrt.
Aus der Base entsteht ein Teilchen, das Protonen abgeben kann, die korrespondierende Säure.
Aufgaben:
1. Definiere Protolyse.
2. Erstelle die Protolysegleichungen von HNO3, HI, H2SO4, H2CO3.
3. Begründe, inwiefern sich die Konzepte von Brönsted und Arrhenius unterscheiden. Treffe dazu eine Fallunterscheidung zwischen den Definitionen von Säure und Base/Lauge.
Ein- und Mehrstufige Protolysen
a) Einstufige Protolysen
HCl + H2O ---> H3O+ + Cl–
Oxonium + Chlorid
HNO3 + H2O ---> H3O+ + (NO3)–
Oxonium + Nitrat
HCN + H2O ---> H3O+ + CN–
Oxonium + Cyanid
H3C-COOH + H2O ---> H3O+ + (H3C-COO)–
Essigsäure Oxonium + Acetat
b) Zweistufige Protolyse von Schwefelsäure
V: Die Leitfähigkeit von Schwefelsäure und Wasser wird einzeln gemessen.
Nun wird vorsichtig etwas Wasser zur Schwefelsäure zugefügt. Die Leitfähigkeit wird gemessen und anschließend ein Diagramm erstellt.
B: Die Leitfähigkeit nimmt zu. Dies geschieht in 2 Stufen.
S: Erst durch die Wasserzugabe findet eine Protolyse statt. Sie geschieht in zwei Schritten, wie man am Leitfähigkeitsdiagramm sehen kann.
Es bilden sich nacheinander die Ionen Hydrogensulfat ((HSO4)-) und Sulfat (SO4)2-.
Säuren, welche mehrere Protonen enthalten wie z.B. Schwefelsäure oder Phosphorsäure geben diese Protonen nacheinander ab:
H2SO4 + 2H2O ---> (HSO4)– + H3O+ + H2O ---> (SO4)2– + 2H3O+
Schwefelsäure Hydrogensulfat Sulfat
Schwefelsäure reagiert also in zwei Schritten zu Hydrogensulfat und Sulfat (beides sind Säurereste!). Beide Säurereste bilden als Feststoff dann entsprechende Salze (z.B. mit Natriumionen NaHSO4 und Na2SO4).
c) Dreistufige Protolyse von Phosphorsäure
Mit Phosphorsäure sind sogar drei Protolysestufen möglich:
H3PO4 + 3H2O ---> (H2PO4)– + H3O+ + 2H2O ---> (HPO4)2– + 2H3O+ + H2O ---> (PO4)3–+ 3H3O+
Phosphorsäure Dihydrogenphosphat Hydrogenphosphat Phosphat
Mit Phosphorsäure kann man dann sogar drei Natriumsalze bilden:
z.B. Natriumsalze: NaH2PO4, Na2HPO4, Na3PO4
Zusatzinformationen:
https://de.wikipedia.org/wiki/Schwefelsäure
https://de.wikipedia.org/wiki/Protolyse
https://de.wikipedia.org/wiki/Phosphorsäure
Die Leitfähigkeit von Säuren
Die Leitfähigkeit einer Flüssigkeit hängt von der Anzahl an vorhandenen Ionen ab. Je mehr Ionen vorhanden sind, desto stärker ist die Leitfähigkeit.
Misst man nun die Leitfähigkeit von konzentrierten Säuren, so stellt man fest, dass sie sehr gering, bis nicht vorhanden ist.
Solange kein Reaktionspartner vorliegt, kann Essigsäure auch keine Protonen abgeben und somit liegen auch keine Ionen vor.

Erst durch Zufügen eines Reaktionspartners, hier Wasser, kann Essigsäure das Proton abgeben, welches dann von Wasser aufgenommen wird. Dabei entstehen zwei Ionen, sodass die Leitfähigkeit schnell steigt.

H3C-COOH + H2O ---> H3O+ + (H3C-COO)–
S B S B
Bei den Edukten:
keine Ionen
⇒ keine Leitfähigkeit
bei den Produkten:
zwei verschiedene Ionen
⇒ Leitfähigkeit
Je mehr Ionen vorhanden sind, desto stärker ist die Leitfähigkeit!
Ein Video zu diesem Versuch findet ihr in meinem Kanal: https://youtu.be/kUqlggvr7yg
Die Autoprotolyse des Wassers
Wasser reagiert mit sich selbst (auto = griech. „sich selbst) in geringem Maße zu Hydroxid- und Oxoniumionen.
H2O + H2O ---> H3O+ + OH–
Allerdings beträgt in neutralem Wasser die Konzentration der Oxoniumionen nur 0,0000001 mol/l [10-7 mol/l]. Dies erklärt auch die (wenn auch geringe) Leitfähigkeit von salzfreiem, destilliertem Wasser (siehe dazu Versuch der Ionenleitfähigkeit).
Wasser reagiert in geringem Umfang mit sich selbst. Dabei entstehen sehr geringe Konzentrationen an Oxoniumionen (H3O)+ und Hydroxidionen (OH)–.
Auch reines Wasser leitet den Strom, welches ein Beweis für die Autoprotolyse des Wassers ist.
Aufgaben:
1. Erstelle wie im oberen Beispiel die zweistufige Protolyse von Schwefliger Säure und dann von Kohlensäure.
2. Notiere die Ionenformel der folgenden Salze: Kaliumhydrogenphosphat, Natriumsulfid, Natriumhydrogensulfit, Natriumhydrogensulfid, Magnesiumhydrogensulfat, Aluminumhydrogensulfat.
Zusatzinformationen:
-
Der Autoprotolysegrad ist dabei von der Temperatur abhängig:
bei 0°C liegen nur 10-7,5 mol H3O+ bzw. OH– vor => pH von 7,5
bei 25°C liegen nur 10-7 mol H3O+ bzw. OH– vor => pH von 7
bei 60 °C liegen nur 10-6,5 mol H3O+ bzw. OH– vor => pH von 6,5
Ist Ammoniak (NH3) eine Lauge?
Eine Messung des pH-Wertes von Ammoniak ergibt einen pH-Wert von ca. 13-14. Dies entspricht dem pH-Wert einer konzentrierten Lauge. Laugen sind wässrige Lösungen von Hydroxidionen (OH)–. Diese sind aber in Ammoniak nicht vorhanden!
Vergleiche typische Laugen mit Ammoniak
- NaOH, KOH => setzen beim Auflösen in Wasser Hydroxidionen (OH–) frei.
- NH3 => setzt bei der Reaktion mit Wasser auch OH– frei, obwohl keines in der Formel vorhanden ist!
Ist Ammoniak (NH3) also eine Lauge, wenn es wie eine Lauge Indikatorpapier blau färbt, aber kein Hydroxid enthält?
Schaut man sich die Reaktion mit Wasser an, kommt man auf die Lösung:
NH3 + H2O ---> NH4+ + OH– +E
NH3 enthält kein Hydroxid, ist also keine Lauge! Aber, es bildet mit Wasser Hydroxidionen. Es reagiert somit alkalisch. Es ist keine Lauge, reagiert aber wie eine. Aus diesem Grunde wurde eine neue Definition notwendig für solche Stoffe, die durch Protonenaufnahme z.B. Hydroxid bilden, aber keine Laugen im eigentlichen Sinne sind.
Da der Begriff „Lauge“ aber schon vergeben war, führten Chemiker den neuen Begriff der „Base“ ein. Basen reagieren alkalisch. Alle Laugen sind auch Basen, da auch sie alkalisch sind und Protonen aufnehmen.
Der Begriff Base umfasst auch hydroxidfreie Stoffe, wie Ammoniak, die alkalisch reagieren.
Die Definitionen lieferte der dänische Chemiker Johannes Nicolaus Brønsted (1879 -1947):
Eine Base ist ein Stoff, der Protonen (=H+) aufnimmt, also ein Protonenakzeptor. Eine Säure ist ein Stoff, der Protonen abgibt, also ein Protonendonator.
Lauge: Eine Lauge ist eine wässrige Hydroxidlösung (OH– in Wasser). Laugen sind gleichzeitig auch Basen. Der Begriff Lauge ist älter und wurde weitgehend durch den neueren Begriff Base ersetzt. Statt „alkalisch“ kann man nun also auch das Adjektiv „basisch“ verwenden.
Ein Video dazu findet ihr in meinem Youtubekanal: https://youtu.be/6ZE4YIXowEA
Zusatzinformationen:
https://de.wikipedia.org/wiki/Ammoniak
https://de.wikipedia.org/wiki/Ammonium
Ist Natronlauge auch eine Base?
Die Reaktion von Natronlauge mit Salzsäure ist ja aus den letzten Kapiteln bekannt. Es ist eine Neutralisation:
NaOH + HCl ---> NaCl + H2O + E
Da es sich bei NaOH und NaCl um Ionen handelt, liegen diese freibeweglich in der Lösung vor:
Na+ + OH– + HCl ---> Na+ + Cl– + H2O + E
Wenn man diese Reaktion so betrachtet, sieht man, dass von NaOH eigentlich nur das Hydroxid (=(OH)–) reagiert hat:
OH– + H+ ---> H2O + E
Natronlauge reagiert mit Wasser, indem es in die freibeweglichen Ionen Na+ und OH– zerfällt. Das Hydroxid vereinigt sich dann im folgenden Schritt mit dem Proton, welches aus der HCl stammt. Es ist also ein Protonenakzeptor und somit eine Base. OH– ist die stärkste Base in wässrigen Systemen.
(Zum Vergleich: H3O+ ist die stärkste Säure in wässrigen Systemen)
Wichtige Hydroxide und ihre Lösungen
|
Formel |
Name der Verbindung |
Name der Lösung |
|
NaOH |
Natriumhydroxid |
Natronlauge |
|
KOH |
Kaliumhydroxid |
Kalilauge |
|
Ca(OH)2 |
Calciumhydroxid |
Kalkwasser |
|
Ba(OH)2 |
Bariumhydroxid |
Barytwasser |
|
Mg(OH)2 |
Magnesiumhydroxid |
--- |
Natronlauge
Natriumhydroxid löst sich gut in Wasser und bildet dabei eine alkalische Lösung. Diese Lösung wird Natronlauge genannt. Natriumhydroxid liegt im Labor meist als Pulver oder in Form von kleinen Plätzchen vor. Auf der Haut fühlen sich solche alkalischen Lösungen in schwacher Konzentration seifig und schmierig an. In starker Konzentration ätzen sie und greifen z.B. organische Stoffe, Fette, Haut und Glas an.
Natronlauge leitet den elektrischen Strom, da sie Hydroxidionen enthält. In Wasser werden diese freigesetzt:
NaOH ----+ H2O---> Na+ + OH–
Diese Reaktion ist stark exotherm, das heißt, es wird Energie freigesetzt und die Lösung erwärmt sich. Da diese Reaktion schon mit der in der Luft enthaltenen Luftfeuchte stattfindet, kann NaOH als Trocknungsmittel verwendet werden, da es durch diese Reaktion der Luft das enthaltene Wasser entzieht.
Eigenschaften von Natriumhydroxid:
- Schmelzpunkt von NaOH: 322°C
- Natriumhydroxid bindet Wasser durch die Reaktion mit H2O => Natriumhydroxid ist hygroskopisch
Bildung von Natronlauge:
Natronlauge entsteht z.B. durch die Reaktion von elementarem Natrium mit Wasser:
2 Na + H2O ---> 2NaOH + H2
Verwendung von Natriumhydroxid:
In Deutschland werden jährlich ca. 4 Millionen Tonnen NaOH benötigt. Es wird in Bäckereien für Laugengebäck, in chemischen Laboren, als Rohrreiniger, zum Beizen von Holz und Holzmöbeln, zur Neutralisation von Säuren, zur Aluminiumherstellung, in Waschmitteln, der Textilindustrie und als Ausgangsstoff für die Reaktionen der chemischen Industrie verwendet.
1844 erfand John Mercer ein Verfahren zum Veredeln von Baumwolle. Dabei werden Baumwollfäden in Natronlauge gegeben, wodurch diese sich verändert und weicher (aber reißfester) und seidiger wird.
Die Säure-Base-Reaktionen (=Protolysen) im Detail
Schaut man sich die Reaktion von Natronlauge mit Salzsäure genauer an und ordnet nun den Stoffen die Begriffe Säure und Base zu, so erlebt man eine Überraschung:
OH– + HCl ---> Cl– + H2O + E
Base + Säure ---> Base + Säure
Bei Säure-Base-Reaktionen wird immer ein Proton übertragen. Es liegt also immer eine Protolyse vor. Des Weiteren sieht man, dass die Base dabei zu einer Säure reagiert und die Säure zu einer Base. Man spricht also immer von einem korrespondierendem Säure-Base-Paar.
Wichtige Beispiele sind: OH– / H2O oder HCl / Cl–
Als Faustregel kann man sich dabei merken:
Starke Säuren reagieren zu schwachen Basen, starke Basen zu schwachen Säuren
Aufgabe:
1. Vervollständige die korrespondierenden Säure-Base-Paare:
|
Säure |
H3PO4 |
HSO4– |
H2O |
NH3 |
||||||
|
Base |
HCO3– |
S2– |
(CO3)2- |
H2O |
Cl– |
HPO42– |
2. Bestimme, ob Säure-Base-Reaktionen vorliegen. Kennzeichne dazu den Übergang der Protonen mit einem farbigen Pfeil und bestimme alle korrespondierenden Säure-Base-Pärchen:
a) H2SO4 + H2O ------>
b) HNO3 + NH3 ------>
c) CaO + H2O ------>
d) H2CO3 + OH– ------> H2O +
e) MgO + Li ------>
Zusatzinformationen:
- https://de.wikipedia.org/wiki/Brönsted
- https://de.wikipedia.org/wiki/Svante_Arrhenius
- https://de.wikipedia.org/wiki/Protonendonator
- https://de.wikipedia.org/wiki/Protonenakzeptor
Ampholyte: Einige Stoffe, können als Säure oder Base reagieren
a) Ammoniak nur als Base oder auch mal als Säure?
Von den vorhergehenden Seiten wissen wir schon, dass Ammoniak alkalisch mit Wasser reagiert. Aber könnte es nicht auch als Säure reagieren?
a) Ammoniak nimmt ein Proton auf (Base), welches mit Wasser dann Hydroxidionen bildet:
NH3 + H2O ----> NH4+ + OH–
Base + Säure ---> Säure + Base
b) Ammoniak gibt ein Proton ab (Säure), welches mit Wasser dann Oxoniumionen bildet:
NH3 + H2O ----> NH2– + H3O+
Säure + Base ---> Base + Säure
Ammoniak ist ein Ampholyt. Ampholyte (als Adjektiv „amphother“) sind Stoffe, die je nach Reaktionspartner als Säure oder als Base reagieren können.
Ein Video dazu findet ihr in meinem Youtubekanal: https://youtu.be/_pjDM4K9_ME
b) Beispiele für weitere Ampholyte:
H2O, NH3, HCO3–, HSO4– , H2PO4– , HPO42– , OH– uvm.
Zuerst einmal ist dies eine theoretische Möglichkeit. Als Schüler kann man natürlich nicht wissen, welche der beiden Reaktionen jetzt abläuft (in der Oberstufe werdet ihr lernen, dass beide Reaktionen ablaufen, eine davon aber mit einer sehr viel höheren Wahrscheinlichkeit ( >99,9%)).
Das Wichtige in diesem Beispiel ist also nicht, was passiert, sondern als Schüler einen Blick dafür zu bekommen, dass es manchmal beide Optionen gibt!
Also:
- NH3 kann als Base oder als Säure reagieren. Beide Reaktionen sind denkbar.
- solche Stoffe nennt man Ampholyt (manchmal auch Amphoter genannt)
- und erst durch ein Experiment kann man bestimmen (also z.B. durch eine pH-Messung), welche Reaktion abläuft.
Aufgaben:
1. H2O kann sowohl als Base (mit HCl) als auch als Säure (mit NH3) reagieren. Erstelle beide Reaktionsgleichungen.
2. Nenne 10 weitere Ampholyte. Tipp: auf den vorherigen Seiten findest Du sogar noch wesentlich mehr.
Wie erkennt man starke und schwache Säuren oder Basen?
Im Labor verwenden Chemiker oft Salzsäure und Schwefelsäure sowie Natronlauge oder Kalilauge. Diese reagieren oft sehr heftig. Wir bezeichnen sie als starke Säuren oder Basen.
Tatsächlich ist es für unerfahrene Chemiker und Chemikerinnen schwer zu erkennen, ob eine Substanz stark oder schwach reagiert. Viele Chemiker und Chemikerinnen wissen dies aus ihrer Laborerfahrung.
Aber es gibt auch einen Trick, mit dem man sich helfen kann. Betrachtet man die folgenden chemischen Reaktionen fällt etwas auf:
H2SO4 + Cl– ---> (HSO4)– + HCl
S B B S
HCl + H2O ---> H3O+ + Cl–
S B S B
NH3 + H2O ---> NH4+ + OH–
B S S B
NH3 + H2O ---> NH2– + H3O+
S B B S
Ich habe starke Säuren und Basen hier mit einem fettgedruckten Buchstaben markiert und sie schwachen Säuren und Basen mit einem Buchstaben, der nicht „fett“ ist.
Wie man bei den korrespondierenden Pärchen nun sieht, reagiert immer eine starke Säure (oder Base) zu einer schwachen Base (oder Säure) und umgekehrt. Eine schwache Säure (oder Base) reagiert zu einer starken Base (oder Säure). Wenn man also ein paar starke Säuren (oder Basen) kennt, dann kann man vieles vorhersagen.
Starke Säuren:
- HF
- HCl
- HBr
- HI
- H2SO4
- HNO3
- H3PO4
Schwache Säuren:
- Essigsäure
- H2S
- H2O
- Ameisensäure
- Zitronensäure
Starke Basen:
- NaOH
- KOH
- NH3
Schwache Basen:
- Ca(OH)2
- H2O
Starke Säuren geben ihre Protonen in Wasser vollständig ab (sie dissoziieren vollständig in Wasser). Schwache Säuren dissoziieren unvollständig.
Es gibt einen speziellen Messwert (pKS-Wert), der dies für Säuren ganz genau angibt. Bitte nicht verwechseln mit dem pH-Wert! Für Basen gibt es den pKB-Wert. Man kann diese Werte für jede Säure und Base nachschlagen. Tatsächlich brauchst Du diese aber erst in der Oberstufe.
pKS < 0 => starke Säure
pKS > 0 => schwache Säure
pKB < 0 => starke Base
pKB > 0 => schwache Base
|
Säurestärke |
pKs |
Säure |
|---|---|---|
|
sehr stark |
−10 |
HClO4 |
|
−10 |
HI |
|
|
−6 |
HCl |
|
|
−3 |
H2SO4 |
|
|
−1,32 |
HNO3 |
|
|
stark |
0,00 |
H3O+ |
|
1,92 |
HSO4− |
|
|
2,13 |
H3PO4 |
|
|
3,14 |
HF |
|
|
3,75 |
HCOOH |
|
|
mittelstark |
4,75 |
Essigsäure |
|
6,52 |
H2CO3 |
|
|
6,92 |
H2S |
|
|
7,20 |
H2PO4− |
|
|
schwach |
9,25 |
NH4+ |
|
9,40 |
HCN |
|
|
10,40 |
HCO3− |
|
|
12,36 |
HPO42− |
|
|
13,00 |
HS− |
|
|
14,00 |
H2O |
|
|
15,90 |
Ethanol |
Noch ein Tipp: Verwechsle nicht verdünnte Säuren mit schwachen Säuren. Eine starke Säure kann man verdünnen, dann wirkt sie schwach. Eine schwache Säure wirkt immer schwach.
Vergleiche dies mit einem Sportwagen, der kann schnell und langsam fahren, ein Kleinwagen hingegen wird auf der freien Autobahn immer langsamer sein als ein Sportwagen.
Zusatzinformationen:
https://de.wikipedia.org/wiki/Starke_Säuren (mit guter tabellarischer Übersicht!)
Die Neutralisation
Erinnere Dich:
-
Durch Neutralisation kann eine Säure durch Lauge unschädlich gemacht werden (und umgekehrt).
-
die ätzende Wirkung der Säure geht vom Wasserstoff bzw. H3O+ aus
-
die ätzende Wirkung der Lauge geht vom OH– (=Hydroxid) aus
=> OH– muss durch H3O+ unschädlich gemacht werden. Zusammen bilden sie H2O.
=> bei einer Neutralisation entstehen immer ein Salz und Wasser.
Reagieren Säure und Lauge miteinander, entsteht dabei immer auch Neutralisationswärme. Dies ist Wäremeenergie, die bei dieser Reaktion frei wird.
Die Neutralisation ist also eine exotherme Reaktion.
Neutralisation von Salzsäure mit Natronlauge
V: Zu Natronlauge wird Universalindikator gegeben und dann tropfenweise Salzsäure hinzugegeben und dabei gut gerührt.
B: Bei genügend Zugabe von Säure verfärbt sich der Indikator. Es entsteht bei gutem experimentellem Geschick eine neutrale Lösung (grüne Farbe des Indikators)
S: In der Natronlauge liegen OH– und Na+-Ionen vor. Hinzu kommen von der Salzsäure H3O+ und Cl–-Ionen. Je mehr man sich dem Neutralpunkt nähert, desto mehr Moleküle H3O+ und OH– reagieren zusammen und bilden Wasser.
Neutralisation: OH– + H3O+ ---> 2H2O + E
Gesamtgleichung: NaOH + HCl + (H2O)2 ---> NaCl + H2O + (H2O) + E
Säuren und Basen sind „Gegenspieler“. Sind genauso viele Teilchen der Säure und der Base in der Lösung vorhanden (also gleiche Konzentrationen), heben sich gegenseitig in ihrer ätzenden Wirkung auf, d.h. sie sind neutralisiert.
Aufgabe:
-
Wenn man nicht weiß, wie viele Teilchen der Säure vorhanden sind, kann man sie durch die Anzahl der Teilchen an Base bestimmen. Aber woher weiß man, wann genauso viele Teilchen vorliegen?
Zweistufige Neutralisation
V: Titration von Schwefelsäure mit Kalilauge (ganz und halb). Anschließend eindampfen der neutralisierten Lösung und der halbneutralisierten Lösung. Vergleich der beiden Salze nach Aussehen und Eigenschaften.
B: Es entstehen zwei Salze, die sich etwas in ihrem Aussehen unterschieden.
S: Nach Zugabe der Hälfte der Kalilauge entsteht v.a. Natriumhydrogensulfat (1. Stufe).
Nach Zugabe der kompletten Menge an Kalilauge ist Natriumsulfat entstanden (2. Stufe).
1. Stufe: NaOH + H2SO4 ---> NaHSO4 + H2O + E
2. Stufe: NaOH + NaHSO4 ---> Na2SO4 + H2O + E
Es entstehen bei beiden Reaktionen ein gelöstes Salz und Wasser.
Gesamtgleichung: 2 NaOH + H2SO4 ---> Na2SO4 + 2 H2O + E
Salzbildung durch Neutralisation
Wie schon einmal im Kapitel „Ionen und Salze“ erwähnt, sind Neutralisationen ein einfacher Weg im Labor Salze herzustellen. Das Säurerestion der Säure und das Metallion bilden dabei gemeinsam das Salz, welches zuerst einmal in gelöster Form vorliegt. Durch Eindampfen erhält man dann das gewünschte Salz in fester Form.
Möchte man zum Beispiel Calciumcarbonat (Kalk) herstellen, lässt man Kalkwasser (= Calciumlauge, enthält Calciumionen) mit Kohlensäure (enthält das Carbonat) zusammen reagieren:
Ca(OH)2 + H2CO3 -----> 2 H2O + CaCO3
Wichtige Salze, welche durch Neutralisation hergestellt werden können:
NaCl:
Vorkommen: Wird als Steinsalz in Bergwerken abgebaut oder aus Meerwasser durch Verdunsten des Wassers gewonnen.
Verwendung: Kochsalz, Konservierungsstoff (Salami, Pökelfleisch) Streusalz, Ausgangsstoff für die Natrium und Chlorgewinnung.
Entsteht z.B. aus Natronlauge, welche mit Salzsäure neutralisiert wird.
NaHSO4
Verwendung: Reinigungsmittel, Säureregulator in Lebensmitteln,
pH-Regulationsmittel, welches den pH-Wert in Schwimmbädern senkt, falls es zu alkalisch wird.
Entsteht z.B. aus Natronlauge, welche mit verdünnter Schwefelsäure neutralisiert wird.
Zusatzinformationen: https://de.wikipedia.org/wiki/Natriumhydrogensulfat
NaHCO3:
Auch Natron genannt.
Dieses Salz setzt bei Kontakt mit Säuren leicht CO2 frei!
Verwendung: Backpulver, Brausepulver, Bestandteil im Schaum von Feuerlöschern, einfacher Stoff zum Neutralisieren (z.B. als Medikament bei saurem Magen und Sodbrennen).
Entsteht z.B. aus Natronlauge, welche mit verdünnter Kohlensäure neutralisiert wird.
Zusatzinformationen: https://de.wikipedia.org/wiki/Natriumhydrogencarbonat
KNO3
Vorkommen: Chilesalpeter
Verwendung: Düngemittel, Bestandteil von Schwarzpulver und Sprengstoffen, Pökelsalz
Entsteht z.B. aus Kalilauge, welche mit verdünnter Salpeterlsäure neutralisiert wird.
CaSO4:
Verwendung: Gips, Kreide, als Baustoff
Entsteht z.B. aus Kalkwasser, welches mit Schwefelsäure neutralisiert wird.
CaCO3
Vorkommen: Kalk, Marmor
Verwendung: Pflanzendünger, Kalkmörtel, Baustoff
Entsteht z.B. aus Kalkwasser, welches mit Kohlensäure neutralisiert wird.
Ca(H2PO4)2
Verwendung: Pflanzendünger
Entsteht z.B. aus Kalkwasser, welches mit verdünnter Phosphorsäure neutralisiert wird.
Aufgaben:
1. Erstelle zu jedem aufgeführtem Salz die zu seiner Bildung (!) passenden Neutralisationsgleichung. (Tipp: um Kaliumnitrat herzustellen, brauchst Du eine Lauge, die Kaliumionen enthält und eine Säure, die Nitrat als Säurerest hat!).
Aufgaben zur Wiederholung
1. Welche der genannten Reaktionen sind Säure-Base-Reaktionen? Kennzeichne bei den Säure-Base-Reaktionen die entsprechenden korrespondierenden Säure-Base-Paare.
O a) Ca + 2 H3O+ ---> Ca2+ + H2 + 2 H2O
O b) (NH4)+ + (OH)– ---> NH3 + H2O
O c) HNO3 + H2O ---> H+ + (NO3)– + H2O
O d) HNO3 + H2O ---> (NO3)– + H3O+
O e) 2 Na + H2O ---> 2OH– + 2 Na+ + H2
2. Vervollständige die folgenden Sätze:
a) Universalindikator dient zur...
b) Der Begriff saure Reaktion beschreibt…
c) Eine Brönstedsäure ist ein…
d) Das Merkmal von Ampholyten ist…
e) Das Kennzeichnen einer Säure-Base-Reaktion ist…
3. Erkläre, wie der Begriff „Lauge“ sich vom Begriff „Base“ unterscheidet und warum eine Neudefinition von Brönsted notwendig war.
4. Mehrstufige Protolysen
a) Bei der zweistufigen Protolyse von Schwefelsäure gibt es zwei verschiedene Säurereste. Nenne sie (mit Namen und Formel)
b) Erkläre den Zusammenhang zwischen der Anzahl an Protonen der Schwefelsäure und der Ionenladung der beiden Säurereste
c) Nenne zu jedem der beiden Säurereste 3 Salze mit ihrer korrekten Formel.
d) Nenne die korrekten Formeln von
Natriumhydrogencarbonat:
Bariumdihydrogenphosphat:
Calciumhydrogensulfid:
Kaliumhydrogensulfit:
Lithiumhydro(gen)oxid:
5. Kreuze die richtigen Aussagen an:
O a) Bei Säure-Base-Reaktionen entstehen immer Oxoniumionen.
O b) Wasser kann als Säure oder Base reagieren. Dies ist vom Reaktionspartner abhängig
O c) Bei der Neutralisation entsteht Reaktionswärme, Salz und Wasser
O d) Säuren greifen unedle Metalle, aber auch Kalk an.
O e) Salzsäure sollte als korrekte Formel „Cl– + H3O+“ auf dem Etikett tragen.
6. Ammonium besteht aus Stickstoff und Wasserstoff (NH4)+. Für Nichtmetalle ist die negative Ladung sehr ungewöhnlich, aber sie ermöglicht Ammonium, als eine der wenigen positiven Nichtmetallverbindungen mit Säureresten Salze zu bilden. Beschreibe eine Reaktion, wie man das Salz Ammoniumchlorid bilden kann.
Titration einer Lauge mit Schwefelsäure
V: Zu 20ml Barytwasser (kaltgesättigt!) wird verdünnte Schwefelsäure getropft (+Universalindikator). Die Leitfähigkeit wird gemessen. Wenn der Neutralpunkt erreicht ist (Farbumschlag), tropft man weiter hinzu! Magnetrührer verwenden!
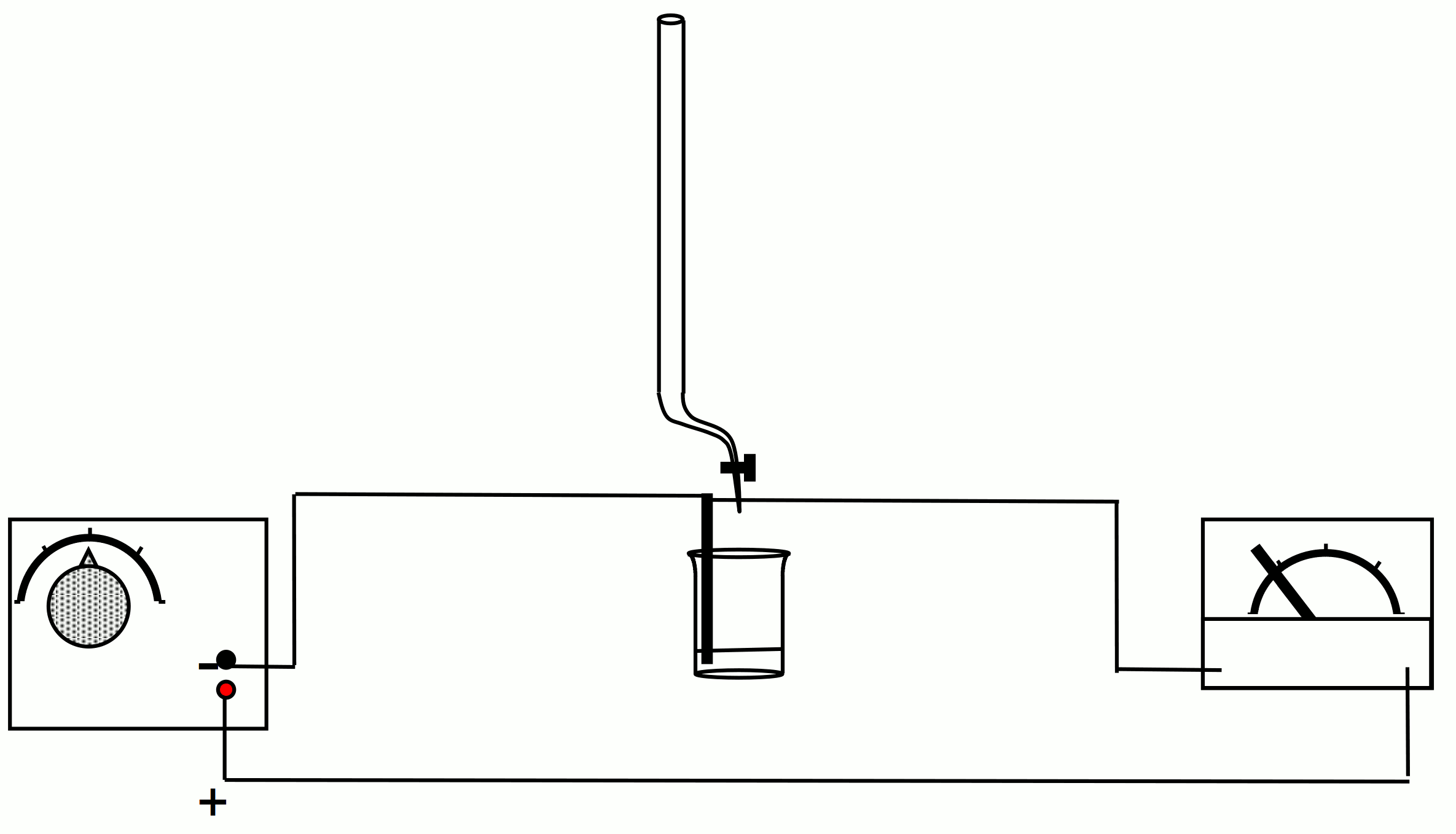
Leitfähigkeitstitration von Bariumhydroxid und Schwefelsäure
B: Die Leitfähigkeit der Lösung nimmt erst ab, dann zu:

|
Vol H2SO4 / [ml] |
I /[A] |
|
0 |
0,001 |
|
1 |
|
|
2 |
|
|
3 |
|
|
4... |
Vol H2SO4 / [ml]
S: Es fand eine Neutralisation statt.
1. Warum leitet Bariumhydroxidlösung den elektrischen Strom?
- In wässriger Lösung zerfällt jedes Molekül Ba(OH)2 in drei Ionen: Ba2+ und 2 OH–. Diese transportieren die elektrischen Ladungen.
2. Warum verringert sich die Leitfähigkeit durch Zugabe von H2SO4?
Ba2+(OH)–2 + H+2SO42– ---> 2 H2O + Ba2+SO42–
1. Ursache: Am Anfang liegen drei Ionen vor. Durch Zugabe von Schwefelsäure verringert sich die Anzahl auf zwei, da zusätzlich Wasser gebildet wird, welche nicht aus Ionen aufgebaut ist.
2. Ursache: Es bildet sich das schwerlösliche Salz BaSO4. Diese leitet nicht den Strom, da es nicht gelöst vorliegt.
3. Warum ist die Leitfähigkeit am Neutralpunkt minimal?
Es liegen keine freibeweglichen Ionen vor!
4. Warum nimmt die Leitfähigkeit dann wieder zu?
Die weitere Zugabe von H2SO4 erhöht die Leitfähigkeit, da dessen Ionen den Strom leiten:
2 H+ + (SO4)2– + Ba2+ + 2 OH– ---> 2 H2O + BaSO4
S: Es bildet sich das schwerlösliche Salz Bariumsulfat, dadurch sinkt die Leitfähigkeit anfangs. Die Protonen werden neutralisiert. Nach Erreichen des Neutralpunktes steigt die Leitfähigkeit, da nun immer mehr Oxonium und Sulfationen hinzukommen und da verdünnte Schwefelsäure nun fast vollständig in Ionen zerfallen ist.
Der pH-Wert
In der 8. bzw. 9. Klasse hast Du gelernt, dass der pH-Wert den „Säuregrad“ angibt. Er wurde Dir als Messgröße mit den Werten 0-14 vorgestellt.
Substanzen mit einem pH-Wert < 7 bezeichnet man als Säuren.
Substanzen mit einem pH-Wert = 7 bezeichnet man als neutral.
Substanzen mit einem pH-Wert > 7 bezeichnet man als Basen/ Laugen.
Nun weißt Du im Gegensatz zu damals aber schon wesentlich mehr über saure Wirkungen von Säuren und Salzen und weißt, dass die Oxoniumionen für die saure, ätzende Wirkung einer Säure verantwortlich sind. Genau diese werden auch mit dem pH-Wert gemessen.
Das Besondere an der pH-Wert Skala ist, dass der Unterschied zwischen einem pH-Wert und dem nächsten das 10-fache beträgt.
Das bedeutet, dass z. B. eine Säure mit pH = 2
zehnmal so sauer wie eine Säure mit pH = 3 ist
und hundertfach so sauer ist wie eine pH = 4 ist.
Um dies genau zu verstehen, musst Du allerdings wissen, was mit dem Begriff „Konzentration“ gemeint ist.
Beachte, dass man das „p“ des pH-Werts klein schreibt!
pH ist Abkürzung für potentia Hydrogenii (Macht/Kraft der Wasserstoffe).
a) Die Konzentration einer Lösung
Die Anzahl an Teilchen (=Stoffmenge) in einer Lösung wird üblicherweise in mol angegeben. Um sie auf die jeweilige Flüssigkeitsmenge zu beziehen, teilt man durch das Volumen:
n
c = ――― [mol/l]
V
b) Definition des pH-Werts
Der pH-Wert gibt die Konzentration von Oxoniumionen an (dies entspricht dem Säuregrad).
Er ist definiert als negativer dekadischer Logarithmus der Konzentration an Oxoniumionen.
=> pH = - lg c (H3O+)
=> c (H3O+) = 10–pH

pH-Papier
Zur Wiederholung aus dem Matheunterricht:
Logarithmen dienen z.B. dazu, Exponenten auszurechnen.
1000 = 103 => lg 103 = 3
100 = 102 => lg 102 = 2
10 = 101 => lg 101 = 1
1 = 100 => lg 100 = 0
0,1 = 10-1 => lg 10-1 = -1
0,01 = 10-2 => lg 10-2 = -2
0,001 = 10-3 => lg 10-3 = -3
Wenn also 1Liter HCl 0,1 mol H3O+ enthält, dann ist die Konzentration 0,1 mol/ l
n 0,1 mol
c = ――― = ―――― = 0,1 mol/l => der pH-Wert ist 1
V 1l
Neutrales Wasser hat, bedingt durch die Autoprotolyse des Wassers, eine H3O+ Konzentration von 0,000 000 1 mol/ l = 10-7 mol/l => pH-Wert = 7
Kann man eigentlich sagen, wie viel mal geringer/ höher die Konzentration an Protonen einer Lösung im Vergleich einer anderen ist?
Ja, denn von pH 1 zu pH 2 ändert sich die Konzentration von 0,1 zu 0,01 mol/l Sie ist also 10 mal geringer. Vergleicht man eine Lösung mit pH = 10 mit einer mit pH = 7, dann ist demzufolge die Konzentration um den Faktor 1000 höher!
Faustregel: Eine pH-Wertstufe entspricht einer Zunahme/ Verringerungder Konzentration um den Faktor 10.
c) Beziehung zwischen dem pH-Wert und dem pOH-Wert
Jetzt könnte man meinen, in Laugen wären keine freien Oxoniumionen vorhanden. Das ist ein Irrtum. Es sind nur sehr wenige. In einer starken Natronlauge befinden sich bei pH-Wert 13 nur 0,000 000 000 000 01 mol/l H3O+.
In der hoch konzentrierten Lauge befinden sich aber sehr viele Hydroxid (OH–) Ionen. Es gilt folgende Beziehung:
pH + pOH = 14
=> wenn also der pH-Wert 13 beträgt, sind 0,000 000 000 000 01 mol/l H3O+ und 0,1 mol/l OH– enthalten.
Mit anderen Worten: In neutralem Wasser liegen 10-7 mol/l H3O+ vor. => pH-Wert ist 7
Wasser ist trotz der H3O+ neutral, da die Konzentrationen CH3O+ und COH- gleich sind (beide 10-7 mol/ l). Bei höheren Protonenkonzentrationen ist die Lösung dann sauer. Bei geringeren ist sie alkalisch, da entsprechend die OH–-Ionen Konzentration zunimmt.
=> pH = - lg c (H3O+); pOH = - lg c (OH–)
=> c (H3O+) = 10–pH; c(OH–) = 10–pOH
d) Beispiele aus dem täglichen Leben

Zusatzinformationen:
Konzentrierte Salzsäure HCl hat eine Konzentration von ca. 12mol/l. Daraus ergibt sich folgende Verdünnungsreihe:
1000ml konz. HCl entspricht 12 mol HCl/l
500ml HCl + 500ml H2O entsprechen 6 mol HCl/l
50ml HCl + 950ml H2O entsprechen 0,6 mol HCl/l
5ml HCl + 995ml H2O entsprechen 0,06 mol HCl/l
2,5ml HCl + 997,5ml H2O entsprechen 0,03 mol HCl/l
Tipps für den Umgang mit konzentrierten Säuren für den Laboralltag:
-
Konzentrierte Schwefelsäure hat eine Konzentration von ca. 18 mol/l.
-
Konzentrierte Salzsäure hat eine Konzentration von ca. 12 mol/l.
Die Stärke von Säuren
Kann man anhand einer Formel eine Vorhersage für die Stärke einer Säure treffen?
Vergleiche dazu mal die Verbindungen Kohlensäure und Methan:

Säuren geben Protonen ab (Protonendonatoren nach Brönstedt). Dabei gilt: starke Säure geben eher ein Proton ab, schwache Säuren tun dies nur in geringem Umfang.
Kann man nun anhand der Valenzstrichformel vorhersagen, ob ein Proton leicht abgegeben wird?
Wie man sieht, ist bei Kohlensäure das Proton an das Sauerstoffatom gebunden und bei Methan an das Kohlenstoffatom. Da Sauerstoff eine hohe Elektronegativität hat, die deutlich höher als die des Kohlenstoffes ist, folgt daraus, dass der die Bindungselektronen zum Wasserstoff viel stärker vom Sauerstoff als vom Kohlenstoff angezogen werden.
=> Wasserstoff ist lockerer an das O gebunden und kann deshalb leichter abgespalten werden.
=> Kohlensäure ist zwar eine schwache Säure, aber sie kann durchaus Protonen abgeben.
Beim Methan hingegen sind die Elektronen fast gleichmäßig verteilt. Die Differenz der Elektronegativitäten beträgt nur ΔEN = 0,3. Die Bindung ist fast apolar. Wasserstoff wird also recht fest an das Kohlenstoffatom gebunden. Eine Abspaltung ist wenig wahrscheinlich.
=> wenn überhaupt, dann wäre CH4 eine sehr sehr schwache Säure. Hinzu kommt, dass Methan ein Gas ist und diese keine Ionen abgeben.
Säuren und Basen im Alltag
Beispiele von pH-Werten bei Alltagsstoffen
|
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|
HCl |
Magensäure,
Kalkreiniger
Batterie- säure |
Zitronensaft |
Essig
Zitronenlimonade |
Cola
Sauerkraut |
Haut
Shampoo
O-Saft |
saure Milch
Speichel |
Leitungs-wasser |
Darmmilllieu
Nordsee- Wasser |
Seife |
nasser Zement |
Waschmittel
Ammoniak |
Kernseife |
Abfluss-frei |
sehr sauer schwach sauer neutral schwach alkalisch sehr alkalisch
Warum ist Milchsäure auf der Haut so wichtig für Menschen?
Der Säureschutz der Haut besteht v.a. aus Harnsäure und Milchsäure. Er verhindert das Eindringen und Wachsen von Bakterien, Viren und Pilzen auf der Haut, da diese in der Regel keine Säure mögen und auch nicht dort wachsen können, wo schon viele Milchsäurebakterien wachsen. Häufiges Duschen oder stark alkalische Seifen „schwächen“ allerdings den Säureschutz.
Wie kommt es zu saurem Regen:
Durch Verbrennung fossiler Brennstoffe entstehen Nichtmetalloxidgase wie z.B. Stickoxide, Kohlenstoffdioxid und Schwefeloxide.
z.B.: 2NO + O2 ---> 2 NO2 + E
3 NO2 + H2O ---> 2 HNO3 + NO + E
NO + NO2 ---> 2 HNO2 + E
Diese Oxide reagieren mit Regenwasser zu Säuren:
z.B.: 2NO2 + H2O ---> HNO3 + HNO2 + E
Indikatorreaktionen als Säurenachweis
Was ist ein Indikator?
Tropfenweise hinzufügen
|
Indikator |
sauer |
neutral |
alkalisch |
|
Lackmus |
|||
|
Phenolphtalein |
|||
|
Bromthymolblau |
|||
|
Methylorange |
|||
|
Tee |
|||
|
Blaukraut |
|||
|
Rote Beete |
|||
|
Johannisbeersaft |
Quantitative Neutralisation
In der Chemie unterscheidet man zwischen qualitativen Verfahren, bei denen die Stoffe an sich bestimmt werden, die an einer Reaktion teilnehmen, oder die dabei entstehen und quantitativen Verfahren, bei denen die Stoffmenge von bekannten Stoffen bestimmt wird.

Um die quantitative Neutralisation zu verstehen, fragen wir uns, wie viel Natronlauge (Konzentration c = 0,1mol/l) man zum Neutralisieren von 10ml HCl mit der Konzentration c = 1mol/l benötigt.
HCl: V= 10ml (=0,01l)
c= 1mol/l
n= ?
Die Stoffmenge n ist leicht zu berechnen:
CHCl = n/ V => n = c · V
=> nHCl = 1 mol/l · 0,01l = 0,01mol
NaOH: V=?
c=0,1mol/l
n= ?
Da wir nicht wissen, welches Volumen NaOH benötigt wird, kann auch nicht die Stoffmenge berechnet werden!
Nützt uns dieses Ergebnis, also die vorhandene Stoffmenge (=Anzahl an Säureteilchen, Oxoniumionen) für HCl um den Wert der Stoffmenge für Natronlauge zu bestimmen?
Ja sicher, denn bei der Neutralisation werden alle Oxoniumionen durch Hydroxid der Lauge unschädlich gemacht. Es muss also gelten:
Im Neutralpunkt ist die Stoffmenge von Oxoniumionen und Hydroxidionen gleich:
nHCl = nNaOH
=> die Stoffmenge an Hydroxidionen (und somit auch an NaOH) ist auch 0,01mol
=> VNaOH = n/c = 0,01mol/ 0,1mol/l = 0,1l (= 100ml)
Damit nun alle Eventualitäten berechnet werden können (also auch z.B., welche Konzentration muss eine Lauge haben, damit genau 100ml verwendet werden), ersetzen wir „n“ in der Gleichung
durch „c · V“.
nHCl = nNaOH
cSäure · VSäure = cLauge · VLauge
Mit dieser Gleichung lassen sich durch Umstellen alle Fälle berechnen! Auf den folgenden Seiten findet ihr jede Menge Beispiel, wie das geht.
In meinem Kanal habe ich drei Videos, die Euch die Titation und die Berechnung erklären:
- Video 1: https://youtu.be/U14RnC8AoM0
- Video 2: https://youtu.be/RxWYiIXoikY
- Video 3: https://youtu.be/U_a-UH53kGQ
Titration einer Salzsäure unbekannter Konzentration (einprotonige Säure)
V: 10 ml Salzsäure (0,2 mol/ l) werden mit einer bestimmten Menge Natronlauge (c = 0,1 mol/l) neutralisiert.
1. Notieren, was gegeben ist, was gesucht ist:
n HCl = ?
c HCl = 0,2 mol/l
V HCl = 0,01 l
n NaOH = ?
c NaOH = 0,1 mol/l
V NaOH =?
2. Reaktionsgleichung aufstellen:
1NaOH + 1HCl ---> 1H2O + 1NaCl + E1
3. Bestimmen der Stoffmengenverhältnisse im Neutralpunkt (=Äquivalenzpunkt)
Dazu genau die Reaktionsgleichung analysieren. Die Zahlen vor der Säure und vor der Base geben den besten Hinweis!
Bedenke: Wenn der optimale Fall eintritt, dass alle Oxoniumionen der Salzsäure mit allen Hydroxidionen der Natronlauge reagiert haben, die Lösung also weder Säure noch Lauge mehr enthält, kann man sagen, dass vorher genauso viele Teilchen HCl wie NaOH vorgelegen haben.
n(HCl) = n (NaOH)
bzw.: nH+ = n (OH)–
bzw.: n(H3O)+ = n (OH)–
=> Im Neutralpunkt gilt nun, dass die Stoffmengen von Oxoniumionen und Hydroxid gleich sein müssen, d.h. das Stoffmengenverhältnis ist 1:1
Stoffmengenverhältnis:
n HCl 1
———— = ― (Ablesen aus der Reaktionsgleichung)
n NaOH 1
n HCl
=> ——— = 1 | · n NaOH
n NaOH
=> n HCl = n NaOH
4. Einsetzten der Formel: n = c · V
=> c HCl · V HCl = cNaOH · VNaOH | : V HCl
=> c HCl = cNaOH · VNaOH / V HCl
5. Überprüfe Dein Ergebnis evtl. durch eine Messung!
Zusatzinformationen:
https://de.wikipedia.org/wiki/Stoffkonzentration
https://de.wikipedia.org/wiki/Titration
Quantitative Neutralisation: Titration einer Natronlauge unbekannter Konzentration
Zu diesem Versuch gibt es ein Video in meinem Kanal: Video 2: https://youtu.be/RxWYiIXoikY
1. Notieren, was gegeben ist, was gesucht ist:
n HCl = 0,0172mol
c HCl = 1 mol/l
V HCl = 0,0172 l
n NaOH = 0,0172mol
c NaOH = 0,688 mol/l
V NaOH = 0,025l
cHCl = n/ V => n = c · V
=> nHCl = 1 mol/l · 0,0172l = 0,0172mol
2. Reaktionsgleichung aufstellen:
1NaOH + 1HCl —> 1H2O + 1NaCl
3. Bestimmen der Stoffmengenverhältnisse im Neutralpunkt (=Äquivalenzpunkt)
Dazu genau die Reaktionsgleichung analysieren. Die Zahlen vor der Säure und vor der Base geben den besten Hinweis!
Im Neutralpunkt ist die Stoffmenge von Oxoniumionen und Hydroxidionen gleich
nHCl = nNaOH
nH3O+ = nOH-
=> Im Neutralpunkt gilt nun, dass die Stoffmengen von Oxoniumionen und Hydroxid gleich sein müssen, d.h. das Stoffmengenverhältnis ist 1:1
Stoffmengenverhältnis:
n HCl 1
———— = ― (Ablesen aus der Reaktionsgleichung)
n NaOH 1
n HCl
=> ——— = 1 | · n NaOH
n NaOH
=> n HCl = n NaOH
cSäure · VSäure = cLauge · VLauge | : VLauge
Auflösen zum gesuchten Wert:
=> c NaOH = cHCl · VHCl / VNaOH
=> c NaOH = 1 mol/l · 0,0172l / 0,025l = 0,688 mol/l
Quantitative Neutralisation: Titration mehrprotoniger Säuren
a) Titration einer zweiprotonigen Säure
Bei mehrprotonigen Säuren (oder Laugen mit mehr als einer Hydroxidgruppe) muss eine Besonderheit beachten:
Beispielaufgabe: Für die Neutralisation von 100,00ml Schwefelsäure benötigt man 75,00ml Natronlauge mit der Konzentration 1,00 mol/l. Bestimme die Konzentration der Schwefelsäure.
Das Problem liegt nun darin, wenn man sich Schwefelsäure (H2SO4) anschaut, dass sie zwei Protonen hat! Pro Proton braucht man ein Hydroxidion. Liegen zwei Protonen vor, so benötigt man auch zwei Hydroxidionen. Wie stellt man nun das Stoffmengenverhältnis auf?
Im Neutralpunkt gilt bei einprotonigen Säuren:
nH+ = n (OH)–
Für zweiprotonige Säuren habe ich in Schulbüchern eine richtige und eine falsche Variante gefunden. Offenbar ist das schwer, das Stoffmengenverhältnis aufzustellen, ohne durcheinander zu kommen.
Was meinst Du, welches Verhältnis ist das richtige?
2 · n(H2SO4) = n (NaOH)
oder: n(H2SO4) = 2 · n (NaOH)
Ein Zwischenschritt erleichtert uns die Lösung:
1. Notieren, was gegeben ist, was gesucht ist:
c H2SO4 = ?
V H2SO4 = 0,100 l
c NaOH = 1,00 mol/l
V NaOH = 0,075 l
2. Reaktionsgleichung aufstellen:
1H2SO4 + 2NaOH ---> Na2SO4 + 2H2O + E
3. Bestimmen der Stoffmengenverhältnisse im Neutralpunkt
Im Neutralpunkt ist laut Reaktionsgleichung die Stoffmenge der Natronlauge doppelt so hoch wie die der Schwefelsäure. Da die Schwefelsäure zweiprotonig ist, liegt die doppelte Menge H3O+ vor:
n H2SO4 1
————— = ― | · 2
n NaOH 2
2 n H2SO4
<=> —————— = 1 | · n NaOH
n NaOH
<=> 2n H2SO4 = n NaOH
4. Einsetzten der Formel: n = c · V
<=> 2 · c H2SO4 · V H2SO4 = cNaOH · VNaOH | : 2 V H2SO4
cNaOH · VNaOH
<=> c H2SO4 = ——————————
2 · V H2SO4
1,00 mol/l · 0,075 l
<=> cH2SO4 = —————————— = 0,375 mol/l
2 · 0,100
b) Titration einer dreiprotonigen Säure
Beispielaufgabe: Für die Neutralisation von 100,00ml Phosphorsäure benötigt man 75,00ml Natronlauge mit der Konzentration 1,00 mol/l. Bestimme die Konzentration der Phosphorsäure.
1. Notieren, was gegeben ist, was gesucht ist:
c H3PO4 = ?
V H3PO4 = 0,100 l
c NaOH = 1,00 mol/l
V NaOH = 0,075 l
2. Reaktionsgleichung aufstellen:
1H3PO4 + 3NaOH ---> Na3PO4 + 3H2O + E
3. Bestimmen der Stoffmengenverhältnisse im Neutralpunkt
n H3PO4 1
————— = ― | · 3
n NaOH 3
3 n H2SO4
<=> —————— = 1 | · n NaOH
n NaOH
<=> 3n H3PO4 = n NaOH
4. Einsetzten der Formel:
<=> 3 · c H3PO4 · V H3PO4 = cNaOH · VNaOH | : 3 V H3PO4
cNaOH · VNaOH
<=> c H2SO4 = —————————
3 V H2SO4
1,00 mol/l · 0,075 l
<=> c H2SO4 = ————————— = 0,25 mol/l
3 · 0,10 l
c) Titration einer Lauge mit zwei Hydroxidgruppen
Beispielaufgabe: Für die Neutralisation von 100,00ml Salpetersäure der Konzentration 0,1 mol/l benötigt man 75,00ml Kalkwasser (Calciumhydroxid). Bestimme die Konzentration der Lauge.
1. Notieren, was gegeben ist, was gesucht ist:
c HNO3 = 0,1 mol/l
V HNO3 = 0,100 l
c Ca(OH)2 = ?
V Ca(OH)2 = 0,075 l
2. Reaktionsgleichung aufstellen:
2HNO3 + 1Ca(OH)2 ---> Ca(NO3)2 + 2H2O + E
3. Bestimmen der Stoffmengenverhältnisse im Neutralpunkt
Im Neutralpunkt ist laut Reaktionsgleichung die Stoffmenge der Natronlauge doppelt so hoch wie die der Schwefelsäure. Da die Schwefelsäure zweiprotonig ist, liegt die doppelte Menge H3O+ vor:
n HNO3 2
—————— = ― | · n Ca(OH)2
n Ca(OH)2 1
<=> nHNO3 = 2·n Ca(OH)2
4. Einsetzten der Formel:
<=> c HNO3 · VHNO3 = 2 · c Ca(OH)2 · VCa(OH)2 | : 2 VCa(OH)2
cHNO3 · VHNO3
<=> ————————— = c Ca(OH)2
2 VCa(OH)2
0,100 mol/l · 0,100 l
<=> ——————————— = 0,066 mol/l
2 · 0,075 l
Hier findet ihr ein Video in meinem Kanal, was die Berechnung nochmal erklärt: https://youtu.be/U_a-UH53kGQ
Zusatzinformationen:
https://de.wikipedia.org/wiki/Stoffkonzentration
https://de.wikipedia.org/wiki/Titration
Aufgaben zur Säure Base Titration und zum pH-Wert
1. Für die Neutralisation von 50,00 ml Schwefelsäure benötigt man 15,00 ml Natronlauge mit der Konzentration 0,10mol/l. Bestimme die Konzentration der Schwefelsäure.
2. 1,50 Liter konzentrierte Salpetersäure mit der Konzentration 4,50 mol/l blieben bei einem Versuch über. Zur Neutralisation steht Natronlauge mit der Konzentration 1,00 mol/l zur Verfügung. Bestimme das notwendige Volumen.
3. 50ml Salzsäure werden mit 30ml Natronlauge (c=0,01mol/l) neutralisiert. Welchen pH-Wert hatte die Salzsäure?
4. Wie viel Natronlauge (c=0,01mol/l) ist zum Neutralisieren eines Mineralwassers (0,75l Flasche) notwendig, wenn der pH-Wert 6,0 beträgt?
5. 0,05 mol einer Schwefelsäure werden auf ein Volumen von 250ml verdünnt. Welche Stoffmenge an Natronlauge ist zur Neutralisation notwendig? ;-)
6. Es sollen 10ml Salzsäure (c= 0,01 mol/l) mit Kalkwasser neutralisiert werden. (Kalkwasser ist eine wässrige Lösung von Calciumhydroxid)
a) Stelle die Reaktionsgleichung auf.
b) Bestimme die notwendige Stoffmenge an Calciumhydroxid.
c) Zur Calciumhydroxid Herstellung liegt Calciumoxid vor. Wie stellt man aus Calciumoxid Calciumhydroxid her (mit Reaktionsgleichung)? (Bedenke: Calciumoxid ist ein Metalloxid)
d) Welche Masse an Calciumoxid muss abgewogen werden, damit die notwendige Stoffmenge an Calciumhydroxid vorliegt?
e) Neutralisiere die Säure, indem Du tropfenweise Dein selbst hergestelltes Kalkwasser hinzufügst. Füge einen Indikator zu und beobachte (In welcher Folge ändert sich die Indikatorfärbung?)
f) Anstelle der Salzsäure werden 10ml Phosphorsäure (c= 0,01mol/l) verwendet. Berechne zuerst das notwendige Volumen an Kalkwasser und dann die notwendige Stoffmenge und Masse an CaO.
7. Definiere pH-Wert und erkläre diese Definition mit Deinen Worten. Erkläre im Anschluss, wie der pH-Wert mit der Hydroxidionenkonzentration in einer Lösung zusammenhängt.
8. Bei einem Experiment bleiben 1,2l Schwefelsäure über. Der pH-Wert ist 1. Wie viel ml Natronlauge (c=0,5 mol/l) sind zum Neutralisieren notwendig?
9. Wie groß ist der pH-Wert (und der pOH-Wert) einer Salzsäure, die eine Konzentration von
a) 1 mol/l hat
b) 0,1 mol/l hat
c) 0,01 mol/l hat
d) 0,001 mol/l hat
e) 0,0234 mol/l hat
10. Wie ist die Konzentration einer Schwefelsäure, welche einen pH-Wert von 4 hat?
11. a) Wie viele Oxoniumionen und wie viele Hydroxidionen befinden sich in 5l Blut, wenn Du weißt, dass Blut einen pH-Wert von 7,4 hat?
b) Wie viele befinden sich in Magensäure (pH-Wert = 1)?
12. a) Welchen pH-Wert hat eine Lösung mit einer Konzentration von 7,1 ·10-3 mol/l?
b) Wie viele Oxoniumionen befinden sich dann in 50ml dieser Lösung?
13. 100ml HCl mit dem pH-Wert=3 werden mit 100ml HCl mit dem pH-Wert 4 zusammen geschüttet. Wie ist der anschließende pH-Wert?
14. Für die Neutralisation von 100ml Kalkwasser steht eine 1molare Phosphorsäure bereit. Es werden genau 22ml der Säure benötigt. Bestimme die Konzentration der Lauge und anschließend den ursprünglichen pH-Wert des Kalkwassers.
15. Im Labor sollen 0,2l einer 0,015 molaren (mol/l) Schwefligen Säure neutralisiert werden.
Zur Neutralisation werden 44 ml Kalkwasser verwendet.
a) Stelle die Reaktionsgleichung auf und bestimme die Namen aller Produkte
b) Welche Konzentration hatte das Kalkwasser?
c) Wie viel Lösung einer 0,1molaren Kalilauge wäre notwendig gewesen?
d) Welchen pH-Wert zeigt ein Liter einer 0,015molaren Schwefligen Säure?
16. Berechne aus dem angegebenen pH-Wert die Konzentration an Oxoniumionen und Hydroxidionen.
a) 4,0
b) 11
c) 4,8
e) 12,55
Musterlösungen
Aufgabe 1
Für die Neutralisation von 50,00ml Schwefelsäure benötigt man 15,00ml Natronlauge mit der Konzentration 0,10mol/l. Bestimme die Konzentration der Schwefelsäure.
1. Notieren, was gegeben ist, was gesucht ist:
n H2SO4 = ? n NaOH =
c H2SO4 = ? c NaOH = 0,1 mol/l
V H2SO4 = 0,05 l V NaOH = 0,015l
2. Reaktionsgleichung aufstellen:
H2SO4 + 2NaOH ---> Na2SO4 + 2H2O + E
3. Bestimmen der Stoffmengenverhältnisse im Neutralpunkt
Im Neutralpunkt ist laut Reaktionsgleichung die Stoffmenge der Natronlauge doppelt so hoch wie die der Schwefelsäure. Da die Schwefelsäure zweiprotonig ist, liegt die doppelte Menge H3O+ vor:
Stoffmengenverhältnis:
n H2SO4 1
—————— = ― | · 2
n NaOH 2
2 n H2SO4
=> —————— = 1 | · n NaOH
n NaOH
=> 2n H2SO4 = n NaOH
4. Einsetzten der Formel: n = c · V
=> 2 (c H2SO4 · V H2SO4) = cNaOH · VNaOH | : 2 V H2SO4
=> c H2SO4 = cNaOH · VNaOH / 2V H2SO4
=> c H2SO4 = 0,1 mol/l · 0,015l / 2 0,05l = 0,015 mol/l
Aufgabe 2:
fehlt
Aufgabe 3:
geg: VS = 50ml = 0,050l
VL = 30ml = 0,030l
cL = 0,01mol/l
ges: cS
Reaktionsgleichung: HCl + NaOH ---> H2O + NaCl
Verhältnis:
nHCl 1 | ∙ nNaOH
————— = ——
nNaOH 1
nHCl = nNaOH
nS = nL
Einsetzten in Formel:
cS ∙ VS = cL ∙ VL | : VS
cS = (cL ∙ VL) : VS = (0,01mol/l ∙ 0,03l) : 0,05l = 0,006 mol/l
Bestimmung pH-Wert: cHCl = cH+ = 0,006 mol/l => pH-Wert = log(0,006) = 2,22
=> Die Salzsäure hatte ca. den pH-Wert 2,22.
Aufgabe 4:
geg: cL = 0,01 mol/l pH = 6 => cs = 0,000001mol/l (aus dem pH-Wert berechnet)
VL = ? Vs = 0,75l
Reaktionsgleichung: 2NaOH + H2CO3 ---> 2H2O + Na2CO3
nS 1 | ∙2 ∙ nNaOH
————— = ——
nNaOH 2
=> 2ns = nL
2cs ∙ Vs = cL ∙ VL | : cL
2cs ∙ Vs
————— = VL
cL
2 ∙ 0,000001 mol/l ∙ 0,75l
VL = —————————————— = 0,00015l
0,01 mol/l
Aufgabe 5:
geg: nS = 0,05 mol ges: nL
1. Reaktionsgleichung: H2SO4 + 2NaOH ---> 2H2O + Na2SO4
2. Verhältnis:
nS 1 | ∙2 ∙ nNaOH
————— = ——
nNaOH 2
<=> 2nH2SO4 = nNaOH
3. Einsetzen: 2 ∙ 0,05mol = nL => 0,1mol = nL
0,1mol Natronlauge sind zur Neutralisation notwendig.
Aufgabe 6:
a) Reaktionsgleichung: Ca(OH)2 + 2HCl ---> 2 H2O + CaCl2 + E
b) Die notwendige Stoffmenge an Calciumhydroxid:
Wie man sieht entsprechen die Stoffmengen sich nicht. Zum Neutralisieren der beiden OH– eines Moleküls Ca(OH)2 braucht man zwei Moleküle HCl:
nLauge 1
—————— = ——
nSäure 2
=> 2nLauge = nSäure
(1) Es gilt also : 2nCa(OH)2 = nHCl
(2) Anzahl an vorliegenden Säureteilchen: nHCl = cHCl · VHCl = 0,001 mol/l · 0,01l = 0,0001mol
aus (1) und (2) folgt => 2nCa(OH)2 = 0,0001mol
=> man benötigt zur Neutralisation also 0,00005 mol Ca(OH)2. Diese reagieren mit 0,0001mol HCl.
c) Wie stellt man aus Calciumoxid Calciumhydroxid dar?
Durch Zugabe von Wasser. Metalloxide und Wasser bilden Laugen!
CaO + H2O ---> Ca(OH)2 +E
d) Welche Masse an Calciumoxid muss abgewogen werden, damit die notwendige Stoffmenge an Calciumhydroxid vorliegt?
Wir benötigen 0,00005 mol Ca(OH)2
=> 0,00005 mol CaO + 0,00005 mol H2O ---> 0,00005 mol Ca(OH)2 +E
=> nCaO = mCaO/MCaO
=> mCaO = nCaO · MCaO = 0,00005 mol · (40,08g/mol + 16,00 g/mol) = 0,0028g
Es müssen 0,0028g CaO abgewogen werden. Diese werden mit einer beliebigen (!) Menge Wasser aufgelöst und für den Versuch verwendet. Sie neutralisieren genau die vorhandene Menge an HCl.
f)
geg: cs = 0,001 mol/l cL = 0,1 mol/l
Vs = 0,010l VL = ?
Reaktionsgleichung: 2H3PO4 + 3Ca(OH)2 ---> 6H2O + Ca3(PO4)2
Verhältnis:
nH3PO4 2 | ∙3 ∙ nCa(OH)2
—————— = ——
nCa(OH)2 3
<=> 3nH2SO4 = 2nCa(OH)2
Berechnung VL:
n= c ∙ V => 3ns = 2nL => 3 ∙ cs ∙ Vs = 2 ∙ cL ∙ VL | :2 : cL
3 ∙ cs ∙ Vs
—————— = VL
2 ∙ cL
3 ∙ 0,001 mol/l ∙ 0,01l
———————————— = VL = 0,00015l Kalkwasser werden benötigt
2 ∙ 0,1 mol/l
Aufgabe 7:
Siehe Definitionen weiter vorne im Kapitel.
Aufgabe 8:
geg: cS = 0,1mol/l (Die Konzentration erhält man aus dem pH-Wert: pH = 1 => 10-1 = 0,1 mol/l)
cL = 0,5mol/l
VS = 1,200l
ges: VL
1. Reaktionsgleichung: H2SO4 + 2NaOH ---> 2H2O + Na2SO4
2. Verhältnis:
nH2SO4 1 | ∙ 2 ∙ nNaOH
—————— = ——
nNaOH 2
<=> 2nH2SO4 = nNaOH
3. In Formel einsetzten:
2 ∙ cS ∙ VS = cL ∙ VL | : cL
VL = 2 ∙ cS ∙ VS : cL = 2 ∙ 0,1 mol/l ∙ 1,2l : 0,5mol/l = 0,48l
=> Es sind 480ml Natronlauge zum Neutralisieren notwendig.
Aufgabe 9:
pH-Werte:
a) 1 mol/l => pH = 0
b) 0,1 mol/l = 10-1 mol/l => pH = 1
c) 0,01 mol/l = 10-2 mol/l => pH = 2
d) 0,001 mol/l = 10-3 mol/l => pH = 3
e) 0,0234 mol/l= 10-1,63 mol/l => pH = 1,63
pOH-Wert:
a) pOH=14
b) pOH=13
c) pOH=12
d) pOH=11
e) pOH=12,37
Aufgabe 10:
Schwefelsäure:
cS = 0,0001 mol/l
Aufgabe 11:
a) Bestimmung der Stoffmenge an Oxoniumionen:
c = 10-7,4 mol/l
V = 5l
=> n = c ∙ V = 10-7,4 mol/l ∙ 5l = 0,000000199 mol
Aufgabe 12:
a) cH3O+ = 7,1∙10-3 mol/l ≈ -2,15 => pH-Wert= 2,15
b)
Gegeben:
c=0,0071 mol/l (siehe oben, aus dem pH-Wert berechnet)
V=0,050l
Einsetzten in Formel: n = c ∙ V = 0,0071 mol/l ∙ 0,05 l = 0,000355 mol
Aufgabe 13:
Man muss für jede Lösung die Anzahl der Oxoniumionen, also die Stoffmenge, berechnen, dann beide Stoffmengen addieren und dann mit dem neuen Volumen von 200ml die neue Konzentration berechnen. Daraus folgt der neue pH-Wert.
n = c · V
Lösung 1:
nH3O+ = 10-3 mol/l · 0,1l = 10-4 mol
Lösung 2:
nH3O+ = 10-4 mol/l · 0,1l = 10-5 mol
Stoffmengen addieren:
nges = n Lösung 1 + n Lösung 2 = 1,1·10-4 mol
Volumen addieren:
Vges = 0,1l + 0,1l = 0,2l
Berechnen der neuen Konzentration:
cges = n ges / Vges = 1,1·10-4 mol/ 0,2l = 5,5·10-4 mol/l
Berechnen des neuen pH-Werts:
pH = - log c(H3O+) = - log 5,5·10-4 = 3,26
Aufgabe 14:
geg: VL = 100 ml = 0,1l Vs = 22ml = 0,022l
cL = ? cs = 1 mol/l
1. Reaktionsgleichung: 3 Ca(OH)2 + 2 H3PO4 ---> 6 H2O + Ca3(PO4)2
2. Verhältnis:
n H3PO4 2 | ∙ 3 ∙ nCa(OH)2
———————— = ——
nCa(OH)2 3
<=> 3nH3PO4 = 2nCa(OH)2
3. Berechnung cL:
n= c ∙ V => 3ns = 2nL => 3 ∙ cs ∙ Vs = 2 ∙ cL ∙ VL | :2 : cL
3 ∙ cs ∙ Vs
—————— = cL
2 ∙ VL
3 ∙ 1mol/l ∙ 0,022l
——————————— = cL = 0,33 mol/l
2 ∙ 0,1l
4. Berechnung pH-Wert:
pH = -log 0,33 = 0,48
Aufgabe 15:
a) Reaktionsgleichung aufstellen:
Schwefelige Säure + Calciumlauge ---> Wasser + Calciumsulfit
H2SO3 + Ca(OH)2 ---> 2H2O + CaSO3
b) Konzentration von Kalkwasser bestimmen
geg: VS = 0,2l ges: cL
cS = 0,015mol/l
VL = 44ml = 0,044l
Verhältnis:
nH2SO3 1 | ∙ nCa(OH)2
——————— = ——
nCa(OH)2 1
<=> nH2SO3 = nCa(OH)2
<=> cS ∙ VS = cL ∙ VL | : VL
<=> cL = cS ∙ VS : VL
Einsetzen: cL = 0,015 mol/l ∙ 0,2l : 0,044l = 0,68 mol/l
Das Kalkwasser hatte die Konzentration 0,68 mol/l.
c) Bestimmung des Volumens der 0,1molaren KOH
geg: VS = 0,2l
cS = 0,015mol/l
cL = 0,1mol/l
ges: VL
1. Reaktionsgleichung: H2SO3 + 2KOH ---> 2H2O + K2SO3
2. Verhältnis:
nH2SO3 1 | ∙ 2 ∙ nKOH
—————— = ——
nKOH 2
<=> 2nH2SO3 = nKOH
3. Formel:
2 ∙ cS ∙ VS = cL ∙ VL | : cL
<=> VL = 2 ∙ cS ∙ VS : cL
4. Einsetzen:
VL = 2 ∙ 0,015mol/l ∙ 0,2l : 0,1mol/l = 0,06l
A: Es wären 0,06l einer 0,1molaren Kalilauge notwendig gewesen.
d) Bestimmen des pH-Werts
pH-Wert = -log(0,015) = 1,82
A: Ein Liter einer 0,015molaren Schwefligen Säure zeigt den pH-Wert 1,82 an.
Aufgabe 16:
a) Oxoniumionen: cH+ = 10-4 mol/l
Hydroxidionen: 1. pOH = 14 - 4 = 10
2. cOH- = 10-10 mol/l
b) Oxoniumionen: cH+ = 10-11 mol/l
Hydroxidionen: 1. pOH = 14 - 11 = 3
2. cOH- = 10-3 mol/l
c) Oxoniumionen: cH+ = 10-4,8 mol/l
Hydroxidionen: 1. pOH = 14 - 4,8 = 9,2
2. cOH- = 10-9,2 mol/l
d) Oxoniumionen: cH+ = 10-12,55 mol/l
Hydroxidionen: 1. pOH = 14 - 12,55 = 1,45
2. cOH- = 10-1,45 mol/l
Zum Üben empfiehlt der Küchenchef heute:
Erstelle für Deine Chemiekartei (Wiederholungskarten) Karten zu folgenden Themen:
-
Atombindung
-
Was ist der Unterschied zwischen einer unpolaren und einer polaren Atombindung?
-
Wie kommt die räumliche Struktur eines Moleküls zustande?
-
die wichtigsten Laugen
-
die wichtigsten Säuren
-
die wichtigsten Metalloxide
-
die wichtigsten Nichtmetalloxide
-
Laugenbildung// Säurebildung
-
Neutralisation
-
Was ist eine Säure, was eine Lauge? Wie kann man sie herstellen?
-
Definiere Atom, Ion, Molekül, chemische Verbindung, Salz, Lösung.
Lösungen:
-
Atom: Teilchen, welches sehr klein ist und bei chemischen Reaktionen ungeteilt bleibt. Atome sind als Elemente im PSE notiert.
-
Ion: geladenes Atom oder Molekül. Die Ladung ist durch Abgabe oder Aufnahme eines Elektrons entstanden.
-
Molekül: Verbindung aus Atomen durch Elektronenpaarbindungen. Die Elektronegativitätsdifferenz der Bindungspartner liegt also bei <1,7.
-
Salz: Feststoffe, welche aus Ionen aufgebaut sind. Die Elektronegativitätsdifferenz der Bindungspartner liegt also bei >1,7.
-
(Chemische) Verbindung: Reinstoff, der aus mehreren, miteinander verbundenen Atomen besteht. Als Bindung kann eine Atombindung oder eine Ionenbindung vorliegen.
-
Lösung: Flüssigkeit (=Lösungsmittel), in der sich ein Stoff aufgelöst hat. Typische gelöste Stoffe sind Salze, Zucker sowie Gase wie z.B. Sauerstoff.
Zusammenfassung: Säure und Laugenbildung
Elemente (Nichtmetalle oder Metalle) bilden bei der Oxidation entsprechend Nichtmetalloxide oder Metalloxide. Diese reagieren mit Wasser zu Säuren oder Laugen. Beide heben sich in der Neutralisation gegenseitig auf. Es entstehen Salze + Wasser!
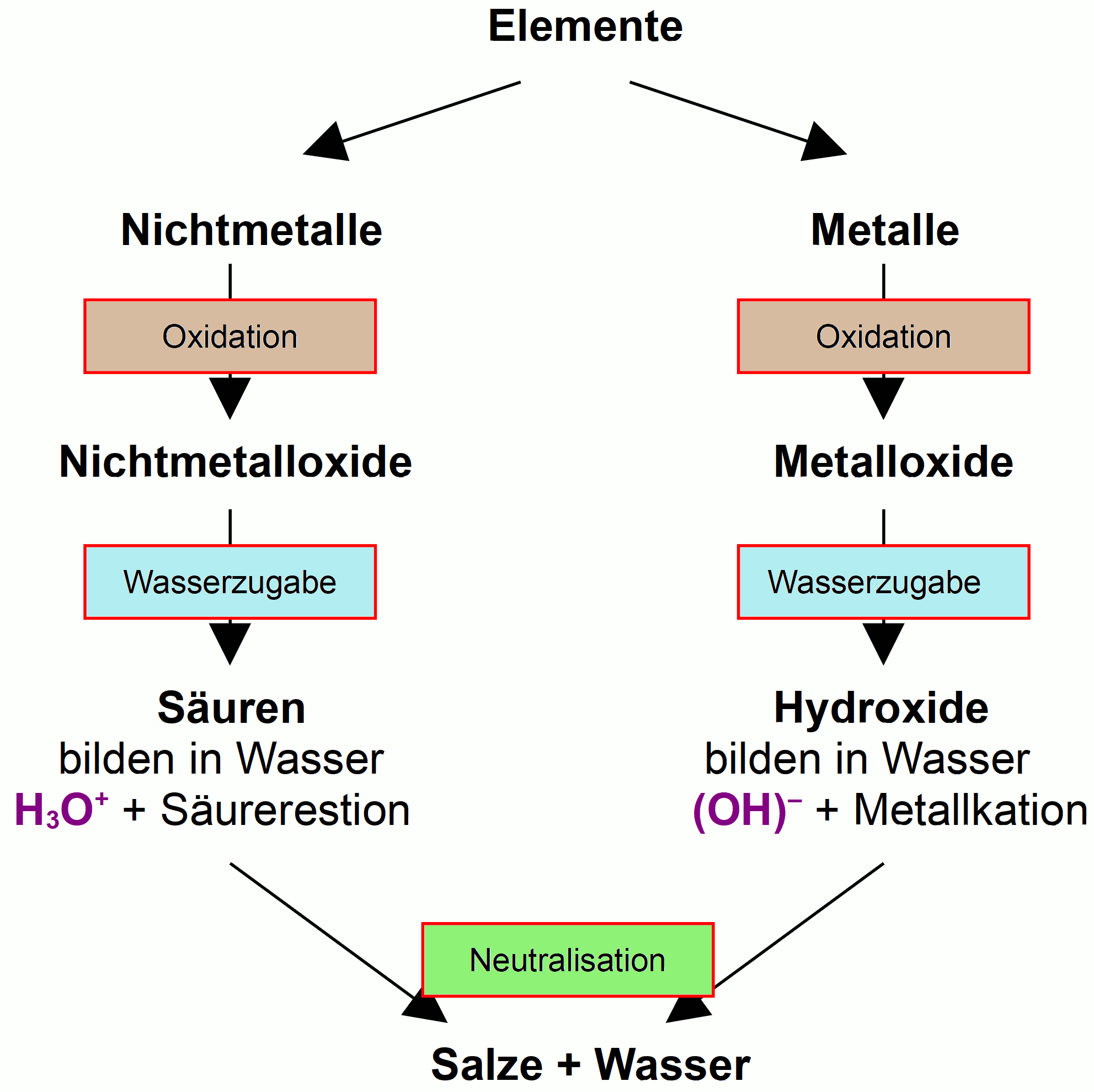
Aufgaben:
1. Fasse die Grafik mit eigene Worten zusammen.
2. Vervollständige die Definitionen mithilfe Deines Heftes / Buches.
Definiere
Arrhenius:
Eine Säure ist...
Eine Lauge ist...
Brönstedt:
Eine Säure ist...
Eine Base ist...
Eine Protolyse ist...
Das Kennzeichen einer Säure-Base Reaktion ist...
Eine Neutralisation ist...
Die Einführung des Konzeptes „Base“ wurde notwendig, da...
Salze entstehen z.B. durch...
Borsäure - eine Säure?
Zeichne die Valenzstrichformel von Borsäure. Beachte dabei folgende Besonderheit, dass alle Wasserstoffe nur mit einer Einfachbindung an das Bor gebunden sind. Formal liegen also OH-Gruppen vor.

Die Kohlensäure und ihre Salze
Stell Dir mal das Öffnen einer Sprudelflasche vor, was für ein Geräusch wirst Du hören? Richtig, das Gas Kohlensäure entweicht. Kohlensäure entsteht, wie Du ja schon weißt aus Kohlenstoffdioxid und Wasser. CO2 besitzt keine Protonen, kann also keine Säure sein! In diesem Versuch wollen wir Kohlensäure etwas besser kennenlernen.
V1: Kohlenstoffdioxid aus der Gasflasche wird durch kaltes Wasser (mit Universalindikator) geleitet.
B1: Der Universalindikator färbt sich rot.
S1: Es fand eine saure Reaktion statt. Das Nichtmetalloxid Kohlenstoffdioxid hat mit Wasser Kohlensäure gebildet.
CO2 reagiert mit Wasser und bildet Kohlensäure: CO2 + H2O ---> H2CO3
Kohlensäure zerfällt in Wasser sofort in Hydrogencarbonat und Protonen (Protolyse), welche dann mit Wasser Oxoniumionen bilden:
H2CO3 reagiert sauer: H2CO3 + H2O ---> (HCO3)- + H3O+
Wegen dieses Zerfalls in Wasser schreibt man die Formel von Kohlensäure oft in Anführungszeichen, da sie in der Form H2CO3 im Grunde nicht stabil ist.
V2: Die in V1 hergestellte Lösung wird im Becherglas erwärmt.
B2: Der Indikator zeigt nach kurzem Erhitzen wieder eine grüne Farbe.
S2: Beim Erwärmen zersetzt sich die Kohlensäure in ihre Bestandteile.
ΔT
H2CO3 ------> CO2 + H2O
Nur 0,1 % des in Wasser gelösten CO2 reagieren mit den Wassermolekülen zur Kohlensäure.
Strukturformeln wichtiger Kohlenstoffverbindungen (ohne freie Elektronenpaare):
O=C=O H-O-C=O –O-C=O
| |
OH O–
Nachweis von CO2 durch Kalkwasser:
Ca2+ + 2 OH– + CO2 + H2O ----> CaCO3 ↓ + 2 H2O
Darstellung von CO2
-
durch Verbrennungen: C + O2 ---> CO2
-
durch Freisetzung aus Carbonat: CaCO3 + HCl ---> CaCl2 + H2O + CO2
Kohlenstoffdioxid ist verantwortlich für „hartes“ Leitungswasser
Kohlenstoffdioxidhaltiges Wasser entsteht in der Natur durch Reaktion von CO2 mit Regenwasser (entsprechend V1). Trifft dieses Wasser auf Kalkstein (Kalk besteht aus dem schwerlöslichen Salz Calciumcarbonat), kann es diesen auflösen.
Bei der Reaktion von Kohlenstoffdioxid, Wasser und Calciumcarbonat entsteht Hydrogencarbonat. Der Kalkstein löst sich dabei auf. Geologen sprechen von der Verwitterung des Kalksteins!
Kohlensäure löst Kalk auf:
Ca2+ + (CO3)2– + H2O + CO2 ---> Ca2+ + 2 (HCO3)– (Säure-Base-Reaktion)
Durch die Freisetzung der Calciumionen, die nun freibeweglich sind, kommt es zur Reaktion dieser Kationen mit den Hydrogencarbonationen. Es entsteht Calciumhydrogencarbonat, welches ein schwerlösliches Salz ist.
Magnesium aus dem Boden kann ebenfalls mit den Hydrogencarbonationen reagieren. Es entsteht Magnesiumhydrogencarbonat, welches ebenfalls ein schwerlösliches Salz ist.
Diese beiden schwerlöslichen Salze bilden zusammen mit Gips aus dem Boden die verantwortlichen Salze, welche für hartes Wasser verantwortlich sind. Diese Salze lagern sich als Rand an Duschen, Töpfen usw. ab.
Für die Wasserhärte sind vor allem CaHCO3, MgHCO3 und CaSO4 (Gips) verantwortlich.
Zusammenfassend werden diese Ablagerungen oft „Kalkablagerungen“ genannt. Man findet sie auf Heizstäben, in Kaffeemaschinen oder Boilern erhöhen den Energieverbrauch, da Kalk die Wärme schlechter leitet. Zu starke Kalkschichten zerstören viele Geräte, wie Wasserkocher, Kaffeemaschinen und Waschmaschinen.
Messung der Wasserhärte:
Früher: 1° deutscher Härte entspricht 10mg CaO in 1l Wasser
heute: siehe Tabelle im Buch
Unterscheide:
- permanente Härte CaSO4
- temporäre Härte CaCO3 (lässt sich durch Erhitzen verringern)
Möglichkeiten der Wasserenthärtung
Beim Waschen reagieren mit der Wasserhärte zu unlöslichen Kalkseifen. Diese haben keine Waschwirkung. In Ionentauschern werden Calcium- und Magnesium-Ionen gegen Natrium-Ionen ausgetauscht.
Unglaublich viele Wiederholungsfragen
Wiederholungsaufgabem Thema "Ionenlehre":
-
Nenne die Regeln, nach denen man die Ionenladung eines Ions bestimmen kann.
-
Beschreibe den Aufbau aller Salze und bilde dann die folgenden Salze:
|
F |
S |
SO4 |
PO4 |
|
|
Na |
||||
|
Ca |
||||
|
Al |
-
Wie bestimmt man die Ladung eines Säurerestes? Welche Ladung hat der Säurerest der Chromsäure „H2Cr2O7“ und welche der der Kieselsäure H2SiO3?
-
Welche Voraussetzungen müssen gegeben sein, damit Ionen den Strom leiten?
-
Auf ein Filterpapier wird in die Mitte eine Linie gezeichnet und darauf blaue Cu2+-Lösung sowie violette MnO4--Lösung getropft. Was passiert, wenn man an die Enden (graue Flächen) eine Spannung von 25V anlegt?
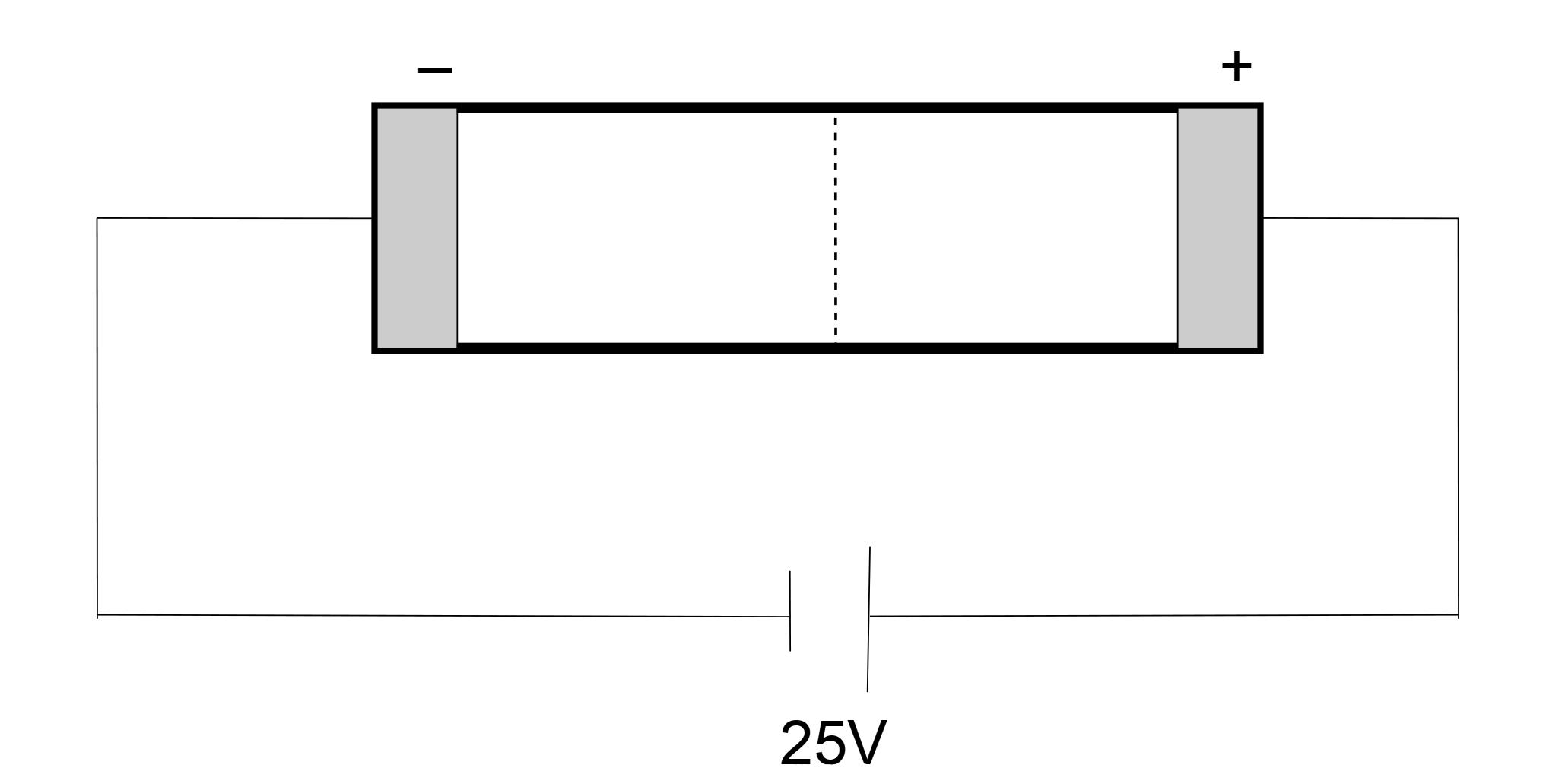
Kathode (-) 25V Anode (+)
-
Nenne mindestens 3 verschiedene chemische Möglichkeiten zur Salzbildung.
-
Was versteht man unter einem Ionengitter? Beschreibe den Aufbau am Beispiel von Kochsalz.
-
Erkläre die Begriffe Koordinationszahl, Ionenbindung und Summenformel.
-
Wovon hängt die Koordinationszahl ab?
-
Beim Lösen von Salzen in Wasser laufen verschieden Vorgänge ab. Erstelle eine Übersicht und erkläre mit dem „Teilchenmodell“ welche Vorgänge ablaufen.
-
Zeichne das Energiediagramm einer exothermen (sowie einer endothermen) Reaktion
-
Kann man eine Vorhersage treffen, ob sich ein bestimmtes Salz exotherm oder endotherm auflöst? Was ist bei schwerlöslichen Salzen?
-
Nenne schwerlösliche Salze und erstelle eine Übersicht, aus der hervorgeht, welche Ionenlösungen man z.B. zusammenkippen kann, um ein schwerlösliches Salz zu bilden.
-
Beschreibe die Verkupferung eines Schlüssels sowie wie man einen Eisennagel verchromt
Wiederholungsaufgabem Thema "Atombindung":
-
Was versteht man unter einer Atombindung? Wie unterschiedet sie sich von einer Ionenbindung?
-
Was ist eine Lewis- bzw. Valenzstrichformel? Was sagt sie aus und wie erstellt man sie?
-
Bei Elektronenpaaren in Valenzstrichformeln gibt es zwei verschiedene Typen. Nenne sie und beschreibe ihre Unterschiede und Gemeinsamkeiten.
-
Wiederhole die Regeln zum Erstellen von Valenzstrichformeln und erstelle dann die Valenzstrichformeln der folgenden Verbindungen: H2, O2, HCl, CH4, H2O, CO2, PF3, SiH4, (ClO4)- sowie die aller Säuren und Säurereste.
-
Was versteht man unter einer Elektronenwolke (=Orbital)?
-
Wie kann ein Element Edelgaskonfiguration erreichen?
-
Sind Moleküle energieärmer oder -reicher als die enthaltenden Elemente?
-
Wovon ist der räumliche Bau von Molekülen abhängig. Wiederhole die Regeln und bestimme den Bau der in Frage 18 genannten Verbindungen.
-
Im Tetraeder liegt ein Bindungswinkel von genau 109,5° vor. Den folgenden Verbindungen liegt ein Tetraeder zugrunde. Folgende Winkel wurden gemessen: CH4 109,5°, NH3 106,8°, H2O 104,5°. Wieso werden die Bindungswinkel kleiner?
-
Bestimme den räumlichen Bau von HClO, HClO2, HClO3, HClO4.
-
Was versteht man unter Elektronegativität? Erkläre und erläutere danach die folgenden Begriffe: polare Atombindung, Partialladung, Dipolmolekül.
-
Zwischen Atom- und Ionenbindung gibt es eine verbindende Beziehung. Erkläre den Zusammenhang und nenne auch eine mathematische Möglichkeit, den Bindungstyp einer Verbindung zu bestimmen.
-
Warum wird ein Wasserstrahl von einer geladenen Folie angezogen?
-
Trotz Partialladungen gibt es Verbindungen, wie z.B. CCl4 oder CO2, die keine Dipolmoleküle sind. Erkläre warum.
-
Welche weiteren Kräfte zwischen Molekülen kennst Du? Nenne sie nach abgestufter Stärke.
-
Bestimme die Bindungsart der folgenden Verbindungen. Bei welchen liegt ein Dipol vor?
CCl4; H2O, HCl; CO2; MgI2; IF6; CBr4; HBr, H2S, AlCl3. -
Welcher Zusammenhang besteht zwischen intermolekularen4 Kräften und Schmelz- und Siedepunkten?
-
Wie kann man Vorhersagen zu den chemischen und physikalischen Eigenschaften von Molekülen treffen?
Wiederholungsaufgabem Thema "Säure, Lauge, Base"
-
Definiere die Begriffe Säure und Lauge und wiederhole alle Säuren und ihr Säurereste.
-
Was ist ein Indikator? Erkläre, welche positiven Eigenschaften ein Stoff haben muss, um ein Indikator zu sein und nenne dir bekannte Indikatoren.
-
Wie kann man Chlorwasserstoff im Labor darstellen? Wie Salzsäure?
-
Was versteht man unter Protolyse? (Autoprotolyse?)
-
Welcher Zusammenhang besteht zwischen Säuren, der Säurewirkung und Oxoniumionen (bzw. Protonen)?
-
Definiere Säure, Lauge/ Base nach Arrhenius und Brönsted. Warum hat Brönstedt das System der Lauge erweitert? (Tipp: nenne zuerst 5 Laugen und 15 Basen!)
-
Warum spricht man bei Säure - Base Reaktionen auch vom „Donator-Akzeptor-Prinzip“?
-
Begründe mit einer Reaktionsgleichung, warum auch NH3 alkalisch wirken kann und OH– freisetzt, obwohl es doch kein Hydroxid in der Formel enthält!
-
Welche Stoffe werden durch Säuren, welche durch Laugen angegriffen?
-
Was versteht man unter dem „korrespondierenden Säure-Base Paar“?
-
Erstelle Gleichungen für die Protolyse von 8 Säuren.
-
Erstelle die Reaktionsgleichung der Reaktion von HF in Wasser. Wie nennt man so einen Protonenübergang?
-
NaHCO3 reagiert mit Wasser und zugegebener Universalindikator zeigt eine blaue Farbe an (alkalisch). Formuliere die Protolysegleichung.
-
NaHSO4 reagiert mit Wasser und zugegebener Universalindikator zeigt eine rote Farbe an (sauer). Formuliere die Protolysegleichung.
-
Was versteht man unter dem pH-Wert? Definiere und erkläre den genauen Zusammenhang zwischen pH-Wert und der Konzentration.
-
Nenne 5 Dinge aus dem täglichen Leben, die eine Säure sind
-
Mit welcher Formel kannst Du berechnen, wie viel Lauge zu einer bestimmten Menge Säure hinzugegeben werden muss.
-
Bestimme die Konzentration einer Lösung, die 95ml Wasser und 1mol Salz enthält
-
Wie viel Wasser muss zu 0,121 mol Kochsalz zugegeben werden, damit eine Lösung mit c = 0,05 mol/l entsteht?
-
Berechne: Es sollen 10ml Salzsäure (c= 0,001 mol/l) mit Kalkwasser neutralisiert. Bestimme die notwendige Stoffmenge an Calciumhydroxid.
-
Berechne: Es sollen 10 ml Phosphorsäure (n= 0,001mol/l) neutralisiert werden. Berechne für Kaliumhydroxid und für Kalkwasser.
-
Definiere Lauge und Base und nenne dann Unterschiede und Gemeinsamkeiten der beiden Konzepte.
-
Definiere den Begriff Ampholyt und nenne fünf Beispiele.
-
10ml Natronlauge unbekannter Konzentration werden mit 250ml Wasser verdünnt. Nun entnimmt man wieder 10ml dieser verdünnten Lauge und neutralisiert diese mit 3,5ml einer 0,1 molaren Salzsäure. Berechne die ursprüngliche Konzentration der Lauge.
-
Schnapp Dir eine kalte Cola, rufe Deinen besten Freund an und entspanne Dich, denn das hast Du jetzt echt verdient ;-)
Fußnoten
1 507 Liter HCl pro Liter Wasser bei 0°C!
2Die Reaktion gelingt nur in Gegenwart von Wasser
3Ausnahmsweise mit der 1 davor, so sieht man besser das die Anteile gleich sind!
4 inter = zwischen, intra = innerhalb